Положение - карбоксильная группа
Cтраница 2
Можно рассматривать также кислоту как углеводород, в котором один или несколько атомов водорода замещены на одну или несколько карбоксильных групп. Положение карбоксильной группы определяется номером углеродного атома главной цепи. [16]
Расщепление оксифлуоренонкарбоновой кислоты ( XI), полученной Бам-бергером и Хукером, окончательно выяснюго этот вопрос. Положение карбоксильной группы, образующейся при разрыве флуоренонового кольца соединения XI при его сплавлении со щелочью, не установлено. [17]
Изменение положения карбоксильной группы с пара на орто у нитробензойных и нитротолуиловых кислот ( нитро - и СН3 - группы в о-положении друг к другу) вызывает при рН 2 резкое смещение волн к отрицательным потенциалам: на 100 и 130 мв соответственно ( [ 273, стр. [18]
 |
Виды ориентации полярных молекул на поверхности.| Схема строения ориентированного граничного слоя. [19] |
На рис. 31 схематически показана структура адсорбированной пленки, построенной из полярных молекул, например жирных кислот с только что рассмотренной зеркальной ориентацией молекулярных рядов. Здесь стрелками обозначено положение полярных карбоксильных групп, вертикальными черточками - направление и длина углеводородных цепей. [20]
Карбоксильные группы в а - и у-положениях диазинов сравнительно легко декарбоксилируются при повышенных температурах. Это свойство может быть использовано для установления положения карбоксильных групп ( стр. [21]
Для двухосновных кислот характерны и некоторые специфические реакции, обусловленные наличием двух функциональных групп. Так, при нагревании они дают различные продукты реакции в зависимости от положения карбоксильных групп. [22]
Это указывает иа больший элект-роноакцепториый эффект фуроксаиового цикла, по-видимому, за счет положительного заряда на атоме азота. Поскольку оба изомера не различаются по кислотности ( при данной точности измерений), то можно предположить, что электронное влияние положительно заряженного азота передается в оба положения карбоксильной группы без больших различий. [23]
Это указывает иа больший элект-роноакцепториый эффект фуроксаиового цикла, по-видимому, за счет положительного заряда на атоме азота. Поскольку оба изомера не различаются по кислотности ( при данной точности измерений), то можно предположить, что электроиное влияние положительно заряженного азота передается в оба положения карбоксильной группы без больших различий. [24]
Поэтому все общие способы получения производных применимы к подобным кислотам. Так например, получение сложных эфиров пирослизевой кислоты может осуществляться без осмо-ления в присутствии серной кислоты, получение хлорангидрида - действием РСЬ на кислоту, хлор - и бромметилирование протекает с хорошими выходами при действии НС1 или НВг и формальдегида и др. Кислоты способны декарбоксилироваться, причем легкость этой реакции зависит от положения карбоксильной группы. Так, пирослизевая кислота легче теряет С02, чем р-фуранкарбоновая. В то же время, если 2 3-дикарбоновая кислота также легко отщепляет в виде СО2 а-карбоксильную группу при нагревании, то у 2, 4-дикарбоновой кислоты для этого же требуется нагревание с медью и хинолином. [25]
Можно рассматривать также кислоту как углеводород, в котором один или несколько атомов водорода замещены на одну или несколько карбоксильных групп. Чтобы назвать кислоту, называют углеводород и добавляют окончание - карбоновая кислота. Положение карбоксильной группы определяется номером углеродного атома главной цепи. [26]
Гидрогенолизу подвергались бенз - и дибензтиофены и ряд тионафте-новых кислот. Усложнение структуры сераорганических соединений обусловливает снижение выхода продуктов гидрогенолиза. Положение карбоксильной группы в непосредственной близости от атома серы также затрудняет гидрогенолиз и снижает выход гид-рюра. Так, глубина гидрогенолиза с 98 % в случае 3-тионафтенуксус-ной кислоты снижается до 85 % для 2-тионафтенуксусной кислоты. Рапа, Швенк и Гинзберг [202] приводят результаты гидрогенолиза метилзамещенных тиофенкарбоновых кислот, сульфида и двух меркаптанов. Тиофенкарбоновая кислота, не имеющая заместителей в тиофеновом кольце, подвергается гидрогенолизу с наибольшей легкостью, введение же в тиофеновое кольцо метильных групп затрудняет гидрогенолиз. Меркаптаны более легко претерпевают реакцию гидрогенолиза, чем сульфиды. [27]
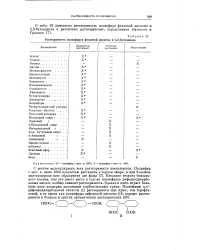 |
Растворимость полиэфиров фталевой кислоты и. 2 3-бутандиола. [28] |
С ростом молекулярного веса растворимость уменьшается. Введение второго бензольного кольца, как это имеет место в случае полиэфиров дифенилдикарбо-новых кислот, вообще снижает растворимость. Однако и здесь играет большую роль изомерия положения карбоксильных групп. [29]
Кислоты жиров окисляются в животном организме до двуокиси углерода и воды. В настоящее время известны все промежуточные стадии этого сложного процесса. Окисление начинается с СН2 - группы, находящейся в - положении относительно карбоксильной группы. [30]
Страницы: 1 2 3