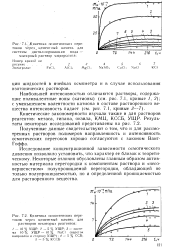
Кинетическая закономерность
Cтраница 1
Кинетические закономерности, характерные для реакции бромирования циклогексена, свойственны и другим реакциям галоидирования олефинов и галоидолефи-нов. Экспериментальные данные, полученные на примере циклогексена, показывают, что образование продукта реакции происходит через активированное состояние, в котором участвуют две молекулы галоида и молекула олефина. Анализ строения промежуточных соединений с участием брома, йода и йодистого брома на атомных моделях приводит к выводу, что образование подобного шестичленного цикла легче всего должно происходить в случае брома. [1]
Кинетические закономерности уже в случае двух последовательных реакций простого типа оказываются значительно более сложными и многообразными, чем для одной реакции простого типа. В реакциях простого типа приходится иметь дело с кинетическими кривыми только для, исходных веществ и конечных продуктов. [2]
Кинетические закономерности, свойственные электрохимическим реакциям, лежат в основе одного из наиболее важных методов исследования и химического анализа, называемого полярографией. Этот метод был разработан чешским электрохимиком Я. Этот метод имеет тесную связь с поляризационными явлениями, наблюдаемыми в ходе электролиза. Химический анализ раствора осуществляется также при помощи поляризационных кривых напряжение - сила тока ( полярограмм), но полученных при специальных условиях. [3]
Кинетические закономерности и механизмы ионной полимеризации имеют более сложный характер, чем в случае радикальной, так как промежуточные активные центры могут сосуществовать в равновесии в виде различных форм: свободных ионов, ионных пар, поляризованных комплексов и др. Смещение этого равновесия в ту или иную сторону путем изменения условий проведения реакций ( температуры, природы растворителя, катализатора и др.) позволяет достаточно активно воздействовать на кинетику процесса и структуру образующегося полимера, что, как правило, исключается в случае радикальной полимеризации. [4]
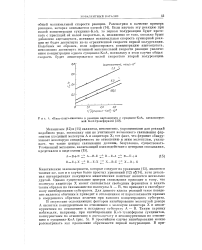 |
Пинг-понг - кинетика в реакции ацетоацетата с сукцинил - КоА, катализируемой КоА - трансферазой. [5] |
Кинетические закономерности, которые следуют из уравнения ( 15), являются такими же, как и в случае более простых урванений ( 12) и ( 14), хотя детальная интерпретация кажущихся кинетических констант является несколько другой. Однако существование центров связывания приводит к тому, что молекула акцептора X может связываться свободным ферментом и влиять таким образом на связывание им молекулы А - В, что приводит к своеобразному ингибированию субстратом. Для данного класса реакций такое поведение является обычным и приводит к отклонениям от параллельности прямых в координатах обратных величин при высоких концентрациях субстрата. В отсутствие осложняющих факторов ингибирование молекулой донора А является конкурентным по отношению к молекуле акцептора X и неконкурентным по отношению к исходному субстрату А - В. [6]
 |
Схема импульсной микрокаталитической установки. [7] |
Кинетические закономерности изучали, изменяя условное время контакта, которое при постоянной температуре и принятой скорости газа-носителя численно равно величине навески катализатора и имеет размерность сек. [8]
Кинетические закономерности в замороженных системах удается объяснить исходя из следующих основных подтвержденных экспериментально положений. Многокомпонентным системам свойственна структурная и фазовая неоднородность; характерно существование твердой и жидкой фаз. В матрице основного вещества компоненты распределены неравномерно, создаются условия для локального концентрирования. [9]
Кинетические закономерности уже в случае двух последовательных реакций простого типа оказываются значительно более сложными и многообразными, чем в случае одной реакции простого типа. В реакциях простого типа приходится иметь дело с кинетическими кривыми всего двух типов. [10]
Кинетические закономерности изучали также и для растворов реагентов: метаса, гипана, окзила, КМЦ, КССБ, УЩР. [12]
Кинетические закономерности при дегидрировании борнеола п изоборнеола - В кн.: Процессы химической технологии древесины и продуктов ее переработки. [13]
Кинетические закономерности перечисленных выше групп основных процессов химической технологии могут быть сформулированы в виде общего закона: скорость процесса прямо пропорциональна движущей силе и обратно пропорциональна сопротивлению. Назвав величину, обратную сопротивлению, коэффициентом скорости, запишем основные кинетические уравнения. [14]
Кинетические закономерности и данные по химическому механизму процесса, установленные для жидкофазного окисления w - бутана, имеют непосредственное значение для других реакций жидкофазного окисления низкомолекулярных парафинов и их смесей. [15]
Страницы: 1 2 3 4