Кинетическая закономерность - окисление
Cтраница 1
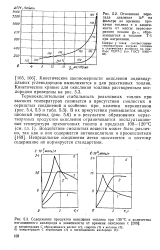
Кинетические закономерности окисления и структура образующихся оксидных пленок на гафнии аналогичны таковым для циркония. При низких температурах изотермы описываются логарифмическим уравнением. Длительность этой стадии уменьшается с ростом температуры. Далее она сменяется стадией окисления по параболическому закону, а затем - стадией линейного окисления. [1]
Кинетические закономерности окисления 1 3-диоксациклоалканов различного строения диоксидом хлора характеризуются первым порядком по обоим реагентам. Исследовано влияние строения 1 3-диоксациклоалканов, полярности растворителя, температуры на скорость реакции. Определены термодинамические характеристики процесса. Предложен механизм реакции 1 3-диоксациклоалканов с диоксидом хлора, лимитирующей стадией которого является образование алкильного радикала. [2]
Кинетические закономерности окисления индивидуальных углеводородов выполняются и для реактивных топлив. [4]
Кинетические закономерности окисления алюминийоргаииче-ских соединений исследованы до настоящего времени недостаточно полно. Скорость окисления алюминийалкилов 4 - 20 описывается дифференциальными уравнения-ми для последовательных реакций первого порядка. [5]
Исследованы кинетические закономерности окисления циклогексена молекулярным кислородом в присутствии ацетилацетонатов скандия, лантана, неодима, никеля, железа, марганца, хрома, меди и кобальта. Предложена общая схема образования основных продуктов окисления - гидроперекиси, окиси, спирта и кетона. Получено уравнение адекватно описывающее общую скорость накопления продуктов реакции ( расходования циклогексена) с учетом стадии гетерогенизации гомогенного катализатора во времени. [6]
Исследованы кинетические закономерности окисления циклогексена молекулярным кислородом в присутствии ацетилацетонатов скандия, лантана, неодима, никеля, железа, марганца, хрома, меди и кобальта. Предложена общая схема образования основных продуктов окисления - гидроперекиси, окиси, спирта и кетона. [7]
Изучены кинетические закономерности окисления циклогексана при различных температурах и давлениях. Обнаружено, что реакция имеет самоускоряющийся характер. Определена общая энергия активации окисления циклогексана, ранная 27 2 ккал / моль, и энергия активации образования гидроперекиси циклогекспла, равная 29 0 ккал / моль. Обнаружено оптимальное давление для окисления цпклогсксаиа. [8]
Исследованы некоторые кинетические закономерности окисления ТВДБМ воздухом в присутствии катализатора ацетата кобальта и бромистого калия в среде уксусной кислоты. [9]
Исследованы некоторые кинетические закономерности окисления ТЩВМ воздухом в присутствии катализатора ацетата кобальта и бромистого калия в среде уксусной кислоты. [10]
Изучены некоторые кинетические закономерности окисления бензилового спирта в среде уксусной кислоты в присутствии ко-бальт-броаидного катализатора. Основными промежуточными продуктами реакции являются банзальдегвд и бен-зилацетат. [11]
Изучены некоторые кинетические закономерности окисления бензилового спирта в среде уксусной кислоты в присутствии ко-бальт-броаидного катализатора. Основными промежуточными продуктами реакции являются банзальдегвд и бен-зилацетат. [12]
Авторами изучены кинетические закономерности гетерогеняо-ка-талитического окисления модельной смеси сульфида натрия кислородом воздуха в присутствии катализатора ТКС. Найдено расчетное уравнение для вычисления скорости реакции окисления сульфиды натрия, предложен механизм реакции. Исследована каталитическая активность и стабильность катализатора ТКС в реакциях окисления сульфиде натрия реальных сернисто-щелочных стоков установок ВД-300, АВТ и термического крекинга Краснодарского я Ново-Горь - ковского НПЗ. [13]
Систематическое исследование кинетических закономерностей окисления пропилена, проведенное в работах [2-7], позволило предположить детальную схему механизма жидкофазного окисления пропилена, включающую стадии образования всех наблюдаемых на опыте кислородсодержащих продуктов взаимодействия компонентов смеси, объясняющие изменение скорости накопления продуктов в ходе процесса. [14]
При рассмотрении кинетических закономерностей окисления этилена на серебряном катализаторе необходимо учитывать, что с изменением химического состава катализатора могут заметно меняться вид кинетических уравнений и различаться значения теплот активации. [15]
Страницы: 1 2 3 4