Ожидаемая закономерность
Cтраница 1
Ожидаемые закономерности в значениях констант скорости часто, но отнюдь не всегда, оправдываются на опыте. Если заряд атакующего иона положительный, как, например, в реакциях енолизации, катализируемых протонами, то с теоретической точки зрения соотношение между константами скорости &2 должно быть обратным: орто мета пара. [2]
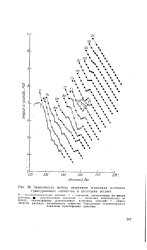 |
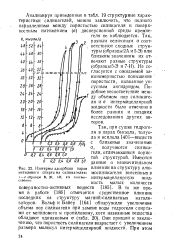
Зависимость между энергиями а-распада изотопов трансурановых элементов и атомными весами. [3] |
Ожидаемые закономерности показаны пунктирными линиями. [4]
Ожидаемые закономерности в значениях констант скорости часто, но отнюдь не всегда, оправдываются на опыте. Если заряд атакующего иона положительный, как, например, в реакциях енолизации, катализируемых протонами, то с теоретической точки зрения соотношение между константами скорости к2 должно быть обратным: орто мета пара. [6]
Отступление от ожидаемых закономерностей можно объяснить только одной причиной: найденные величины относятся не к бимолекулярным реакциям, а к сумме двух последовательных реакций, из которых одна является общей и равновесной. [8]
 |
Изотермы адсорбции паров ВЛИЯНИИ на структуру алю-метилового спирта на силикагелях. МОСИЛИКагеля внесенных В. [9] |
Не согласуется с ожидаемой закономерностью повышение пористости, вызванное уксусным ангидридом. Подобное несоответствие меж - ду объемом пор силикагеля и а иитермицеллярной жидкости было отмечено в более ранних и поздних исследованиях других авторов. [10]
Кислотность оксокарбоновых кислот характеризуется ожидаемыми закономерностями ( табл. 9.5.1), и поскольку анион-стабили-зующий индуктивный эффект карбонильной группы быстро затухает по мере удаления от карбоксильного центра, 5-оксогексано-вая кислота лишь немного, сильнее, чем гексановая. [11]
Никогда не следует переоценивать согласие экспериментальных данных с ожидаемыми закономерностями. Необходимо всегда относиться критически не только к чужим, но в первую очередь и к собственным результатам и теоретическим выводам. [12]
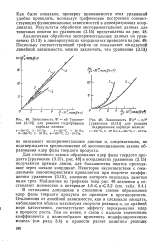 |
Зависимость W - n / t [ уравне - [ IMAGE ] Зависимость Wjt3 - n / t3 ние ] для реакции гидрирования [ уравнение ] для реакции. [13] |
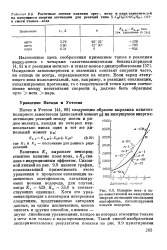
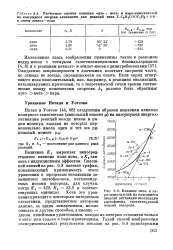
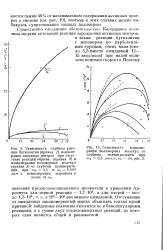
Для степенного закона образования ядер фазы твердого продукта [ уравнение (3.15), рис. 48 ] в координатах уравнения (3.15) получаются прямые линии, для большинства опытов проходящие через начало координат. Некоторое несоответствие с ожидаемыми закономерностями проявляется при подсчете коэффициента уравнения (3.15), значения которого оказались заметно ниже трех. [14]
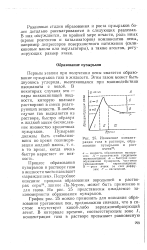 |
Изменение концентрации газа в растворе, образование пузырьков и рост ячеекзг. [15] |
Страницы: 1 2 3