Бутантиол
Cтраница 2
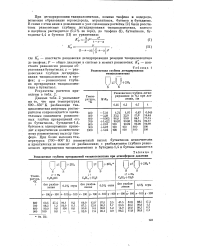 |
Равновесные глубины превращений тиациклопентана при атмосферном давлении. [16] |
Лр - константа равновесия дегидрирования реакции тиациклопентана до тиофена; Р - общее давление в системе в момент равновесия; K V - - константа равновесия реакции образования бутантиола; - равновесная глубина дегидрирования тиациклопентана в тио-фен; у - равновесная глубина превращения тиациклопентана в бутантиол. [17]
На примере бутантиола показана эффективность метода Г1Х при 93i или 60 - 180 на капиллярной колонке с НФ - силанокс-101, карбовакс 20М и аптет-80. Подводящий капилляр обрабатывают раствором бензотриазола в ацетоне. [18]
Практически нерастворим в воде, хорошо растворяется в органических растворителях. Обладает неприятным запахом бутантиола. [19]
Реакция с тиофенолом идет с малой скоростью даже при l O0 С в присутствии mpem - бутилпероксида. Добавка тиофенола в систему триэтилфосфит - бутантиол ингибирует реакцию. [20]
Загрузка: н-гептан Ч - w - бутантиол ( содержание серы в смеси 0 097 % вес. [21]
Для других классов соединений может наблюдаться, однако, и противоположный характер зависимости к от способности группы ХН к образованию Н - связей. При резком увеличении под влиянием электроотрицательных заместителей протонодонорной способности молекулы трифторэтанола константы скорости его Н - обмена с бутантиолом не отличаются от величин к для метанола. [22]
Для других классов соединений может наблюдаться, однако, и противоположный характер зависимости k от способности группы ХН к образованию Н - связей. При резком увеличении под влиянием электроотрицательных заместителей протонодонорной способности молекулы трифторэтанола константы скорости его Н - обмена с бутантиолом не отличаются от величин k для метанола. [23]
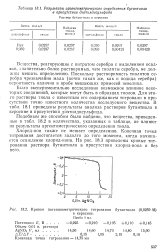 |
Результаты аргентометрического определения бутантиола.| Кривая потенциометрического титрования бутантиола ( 0 0259 М. [24] |
Было экспериментально исследовано возможное влияние некоторых соединений, которые могут быть в образцах тиолов. В табл. 18.1 приведены результаты анализа растворов бутантиола в керосине в присутствии диэтилдисульфида. [25]
Хлорид-ион также не мешает определению. Конечная точка титрования достигается задолго до того момента, когда начинается осаждение хлорид-иона. На рис. 18.3 приведены кривые титрования раствора бутантиола в присутствии хлорид-иона и без него. [26]
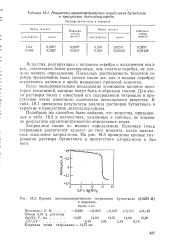 |
Результаты аргентометрического определения бутантиола.| Кривая потенциометрического титрования бутантиола ( 0 0259 М. [27] |
Было экспериментально исследовано возможное влияние некоторых соединений, которые могут быть в образцах тиолов. В табл. 18.1 приведены результаты анализа растворов бутантиола в керосине в присутствии диэтилдисульфида. [28]
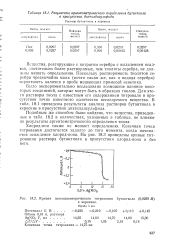 |
Результаты аргентометрического определения бутантиола.| Кривая потенциометрического титрования бутантиола ( 0 0259 М. [29] |
Хлорид-ион также не мешает определению. Конечная точка титрования достигается задолго до того момента, когда начинается осаждение хлорид-иона. На рис. 18.3 приведены кривые титрования раствора бутантиола в присутствии хлорид-иона и без него. [30]
Страницы: 1 2 3