Третичный бутилбензол
Cтраница 2
Октан может быть практически полностью превращен в изобу-тан и третичный бутилбензол. Эти хлориды реагируют как настоящие катализаторы, так как 1 моль их может вызвать превращение не менее 20 молей октана. Реакции способствует присутствие хлористого водорода. Попутно установлено, что А1С13 и ZrQ4 частично образуют с ароматическими углеводородами тестообразные или жидкие коричнево-красные продукты присоединения. [16]
Действием серной кислоты, содержащей небольшое количество серного ангидрида, удалось превратить вторичный бу-тилбензол [70], третичный бутилбензол [71], несколько изомерных амилбензолов [72, 73], гексдлбензолов [ 74 а-г ], а также и-октил-бензол [ 74 д ] в соответствующие сульфокислоты, несомненно, представляющие собой иара-изомеры. Впрочем, прямого доказательства этого не получено, за исключением неопентилбензола [73], из которого с 95 % - ным выходом синтезирована л-сульфо кис лота, превращенная путем окисления в соответствующую бензойную кислоту. Образование о-сульфокислот в указанных реакциях незначительно. Гексадецил и н-октадецилбензолы с олеумом [ 75 а ] также дают л-сульфокислоты, строение которых установлено путем сплавления со щелочью. [17]
Действием серной кислоты, содержащей небольшое количество серного ангидрида, удалось превратить вторичный бу-тилбензол [70], третичный бутилбензол [71], несколько изомерных амилбензолов [72, 73], гексилбензолов [ 74 а-г ], а также и-октил-бензол [ 74 д ] в соответствующие сульфокислоты, несомненно, представляющие собой пара-изомеры. Впрочем, прямого доказательства этого не получено, за исключением неопентилбензола [73], из которого с 95 % - ным выходом синтезирована л-сульфокислота, превращенная путем окисления в соответствующую бензойную кислоту. Образование о-сульфокислот в указанных реакциях незначительно. Гексадецил и w - октадецилбензолы с олеумом [ 75 а ] также дают п-сульфокислоты, строение которых установлено путем сплавления со щелочью. [18]
Из ароматических углеводородов наибольшей детонационной стойкостью обладают мезитилен ( 1 3 5-триметилбензол), изопро-пилбензол и третичный бутилбензол. Среди ароматических углеводородов отрицательную детонационную стойкость на богатой смеси имеет ортоксилол. [19]
 |
Состав реакционной смеси. [20] |
Фракция, кипящая при 169 - 172, содержала 28 - 30 % вторичного и 70 - 72 % третичного бутилбензола. [21]
Подобным же образом из нормального бромистого бутила и бензола получается вторичный бутилбензол, а из бромистого изобутила и бензола - третичный бутилбензол. [22]
Как было показано в подразделе 2, § 2, среди исследованных соединений симметрия я-электронного облака бензольного кольца меньше всего отклоняется от правильной шестиугольной формы, присущей свободной молекуле бензола, у третичного бутилбензола. Связано это с тем, что в заместителе третичного бутилбензола система rr - электронов С - Н - связей, которая может участвовать в гиперконьюга-ции с я-электронами бензольного кольца, отделена от последнего четвертичным атомом углерода. [23]
В настоящем разделе приведены сведения об ультрафиолетовых спектрах поглощения при низких температурах пятнадцати монозамещенных бензола, синтезированных в основном в ИОХ АН СССР: этилбензола, н-пропилбензола, ку-мола, н-бутилбензола, зо-бутилбензола, третичного бутилбензола, н-гексилбензо-ла, 2-метил - 3-фенилпропена - 1, аллилбен-зола, фенилциклопропана, транс-и цис-1 - фенил - 2 - циклопропилциклопропанов, 2-метил - 1-фенилпропена - 1, стирола и полистирола. [24]
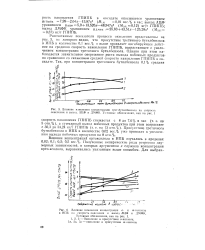
Рассчитанные показатели процесса окисления представлены на рис. 3, из ( Которого видно, что присутствие третичного бутилбензола-в ИПБ в количестве 0 1 вес. ГПИПБ, возрастающее с увеличением концентрации третичного бутилбензола. Однако при этом наблюдается значительное опережение роста выхода побочных продуктов, по сравнению со снижением средней скорости накопления ГПИПБ в оксидате. [26]
ГПИПБ, возрастающее с увеличением концентрации третичного бутилбензола. [28]
Как было показано в подразделе 2, § 2, среди исследованных соединений симметрия я-электронного облака бензольного кольца меньше всего отклоняется от правильной шестиугольной формы, присущей свободной молекуле бензола, у третичного бутилбензола. Связано это с тем, что в заместителе третичного бутилбензола система rr - электронов С - Н - связей, которая может участвовать в гиперконьюга-ции с я-электронами бензольного кольца, отделена от последнего четвертичным атомом углерода. [29]
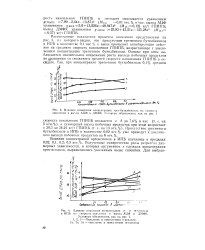
Спектр раствора третичного бутил-бензола в 2 2 4-третшшентане при 293 К [43] также состоит из ряда широких полос. Частотные интервалы, найденные из спектров раствора и аморфного третичного бутилбензола, близки друг к другу. [30]
Страницы: 1 2 3 4