Бутилгидроперекись
Cтраница 1
Бутилгидроперекись является устойчивой по отношению ко многим сильным кислотам. Однако, как показывает наш опыт, эта гидроперекись в растворе бензола в присутствии бензолсульфо-кислоты уже при комнатной температуре претерпевает превращение, которое можно наблюдать визуально по помутнению реакционной смеси и последующему ее расслоению. Алкалиметрическое определение концентрации бензолсульфокислоты в реакционной смеси после завершения разложения грег-бутилгидроперекиси показало, что кислота в реакции не подвергается необратимому превращению. Это дает основание считать, что бензолсульфокис-лота в исследованной нами реакции действительно играет роль катализатора. [1]
Бутилгидроперекись расходуется в процессе синтеза в соответствии с кинетическим уравнением реакции второго порядка. Это отвечает пропорциональности скорости реакции концентрациям гидроперекиси и изоолефина в первой степени. Стадия образования карбоний-иона из олефина и кислоты по реакции ( 1) в нашей системе проходит сравнительно быстро и успевает достигнуть равновесия. [2]
 |
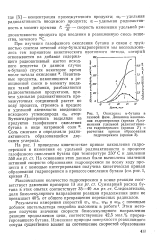
Зависимость выхода продуктов газофазного окисления н-бутана от температуры. / - олефины. 1-кислородсодержащие соединения. [3] |
Бутилгидроперекись устойчива и может быть выделена из продуктов реакции. [4]
Бутилгидроперекись и ди-трег-бутилперекись находят промышленное применение в качестве инициаторов радикальной полимеризации и при вулканизации полиолефиновых каучуков. [5]
Бутилгидроперекись является устойчивой по отношению ко многим сильным кислотам. Однако, как показывает наш опыт, эта гидроперекись в растворе бензола в присутствии бензолсульфо-кислоты уже при комнатной температуре претерпевает превращение, которое можно наблюдать визуально по помутнению реакционной смеси и последующему ее расслоению. [6]
Бутилгидроперекись расходуется в процессе синтеза в соответствии с кинетическим уравнением реакции второго порядка. Это отвечает пропорциональности скорости реакции концентрациям гидроперекиси и изоолефина в первой степени. Стадия образования карбоний-иона из олефина и кислоты по реакции ( 1) в нашей системе проходит сравнительно быстро и успевает достигнуть равновесия. [7]
Термическое разложение третичной бутилгидроперекиси катализируется дитретичными перекисями и протекает цепным путем. При проведении этой реакции с перекисью ( СН3) зСООО при температуре 195 в присутствии эквимолекулярного количества дитретичной бутилпере-киси Себолд, Раст и Воган [682] обнаружили в продуктах реакции мо-нодейтерометан СНзО, а при проведении реакции в присутствии дитретичной амилперекиси - этан, также содержащий дейтерий. [8]
Разложение rper - бутилгидроперекиси 194 в мономерных растворителях ускоряется акцепторами протонов, такими, как бензил, ди-ацетил и другие поликетоны, поэтому предложена новая система для интенсификации полимеризации олефинов: гидроперекись - кетон. Вообще в среде олефинов 19 энергия активации распада алкилгидроперекисей снижается от 35 до 28 ккал / моль. [9]
При применении mpem - бутилгидроперекиси в качестве окислителя для различных алкильных реактивов Гриньяра выходы спиртов в расчете на израсходованную гидроперекись составляют 90 - 99 % [9]; см. также гл. [10]
Присоединение к альдегидам и кетонам mpem - бутилгидроперекиси приводит к получению пероксисоединений, построенных по типу ацеталей. [11]
Ниже представлены результаты окисления изоамилацетата в присутствии mpem - бутилгидроперекиси ( 1 5 вес. [12]
 |
Окисление н-бутана в. [13] |
При изучении газофазного окисления бутана в связи с трудностью синтеза меченой srop - бутилгидроперекиси мы воспользовались тем вариантом кинетического изотопного метода, который основывается на добавке содержащего радиоактивный изотоп исходного вещества ( в данном случае я-бутана) спустя некоторое время после начала окисления и. Неактивные продукты, накопившиеся в реакционной смеси к - моменту введения такой добавки, разбавляются радиоактивными продуктами, причем удельная радиоактивность промежуточных соединений растет по ходу процесса, стремясь в пределе к удельной активности введенного исходного углеводорода ао. [14]
Для инициирования окисления в реакционную среду добавляют некоторое количество перекиси водорода или mpem - бутилгидроперекиси. При оптимальных условиях реакция протекает в слабокислой среде. Поддерживать эти условия можно, добавляя в реактор неорганические или органические кислоты. Для стабилизации перекиси водорода в реакционную смесь добавляют такие вещества, как щелочные пирофосфаты. [15]
Страницы: 1 2 3