Бутилгидроперекись
Cтраница 3
Таким образом, различие исследуемых соединений по термической устойчивости определяется прежде всего различием энергии активации их термического распада. Наблюдаемые периоды быстрого распада гидрата соли rper - бутилгидроперекиси при повышенной температуре, вероятно, отвечают распаду не самого гидрата, а неизвестного промежуточного продукта его превращения. [31]
Разница в оптических плотностях поглотительного раствора до и после пропускания воздуха, определяемая при А412 нм ( е7700), пересчитывается на озон с учетом того, что реакция окисления ДДЛ стехиометрична. Перекись водорода и органические перекиси ( на примере бутилгидроперекиси) в обычно присутствующих в атмосфере концентрациях на результаты анализа не влияют. Метод отличается простотой, однако его серьезным недостатком является очень низкая чувствительность - для определения природного содержания озона в воздухе необходим 2 - 3-часовой отбор проб. [32]
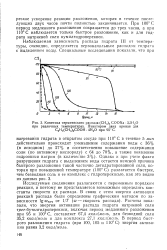 |
Кинетика термического распада ( СН3 3 COONa 3 5Н2О. [33] |
Исследуемые соединения разлагаются с переменным порядком реакции, и поэтому не представляется возможным определить константы скорости их распада. Расчеты показали, что энергия активации распада гидрата натриевой соли rper - бутилгидроперекиси, включая период медленного разложения при 95 и 100 С, составляет 67 4 ккал / моль, для безводной соли 35 2 ккал / моль и для комплекса 27 1 ккал / моль. В период быстрого разложения гидрата ( при 100, 105 и 110 С) энергия активации равна 3 2 ккал / моль. [34]
Смете, Пут, Мюллер и Беке [330] получили привитые сополимеры полиметилметакрилата, содержавшего трет, бутилперо-ксидные группы. Исходный полимер был получен сополимери-зацией метилметакрилата с акрилхлоридом, с последующим замещением хлора действием трет, бутилгидроперекиси. [35]
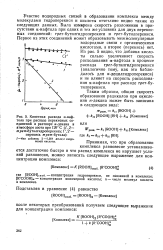 |
Кинетика - расхода а-нафтола при распаде перекисных соединений в растворе н-декана в или атмосфере азота при 120 С ( /, 2. [36] |
Участие водородных связей в образовании комплекса между молекулами гидроперекиси и кислоты отчетливо видно также из следующих данных. Была измерена скорость разложения в присутствии а-нафтола при одних и тех же условиях для двух перекис-ных соединений: г / 7ег - бутилгидроперекиси и грег-бутилперекиси. [37]
Синтезировано 16 перекисей пяти различных типов: гидроперекиси гептана, изооктана, метил-циклогексана, толуола, этилбензола, бутилбензола, тетралина [2, 3], трет, бутилгидроперекись [4]; перекиси метила [5] и ди-трет. [38]
 |
Энергия разрыва связей в молекулах, ккал / моль. [39] |
Как видно из данных табл. 1, некоторые типы связей ( I-I, F-F, О-О) сравнительно непрочны. Например, образование свободного радикала ОН из воды с разрывом связи Н - ОН требует затраты энергии 116 ккал / моль, образование того же свободного радикала из перекиси водорода с разрывом связи НО-ОН - 49 6 ккал / моль, а из / npem - бутилгидроперекиси с разрывом связи ( СН3) 3СО - ОН - 39 ккал / моль. [40]
В работах настоящего сборника описаны многие реакции ал-килгидроперекисей с различными веществами. Показано, что трет-бутилгидроперекись реагирует с уксусным ангидридом в присутствии уксусной кислоты с образованием грег-бутилперацетата; интересно, что эта реакция инициируется ацетатом кобальта. Уточнены условия взаимодействия rper - бутилгидроперекиси с изобути-леном, приводящего к перекиси грег-бутила. Изучена реакция ку-милгидроперекиси с ароматическими аминами с образованием молекулярных соединений с анилином, а - и ( З - нафтиламинами. Установлено, что кумилгидроперекись в водных растворах под влиянием бромистого н-алкилпиридиния претерпевает радикальное окислительно-восстановительное превращение. [41]
Совершенно новый способ изменения природы основной цепи был избран Тобольским и Рембо [4], которые получили блоксополи-меры полиуретана и полистирола. Сначала был синтезирован пре-полимер на основе полиэтиленпропиленадипнната и ТДИ. Затем, при взаимодействии его с / npem - бутилгидроперекисью получают пер-карбамат, который смешивают со стиролом и нагревают в течение 24 ч при 73 С. В этих условиях перкарбамат, очевидно, разлагается, с образованием свободного радикала на каждом конце полимерной цепи, который затем инициирует полимеризацию стирола. [42]
Исследование ассоциации гидроперекисей должно помочь лучшему пониманию их физических и химических свойств. Однако соответствующих работ, в частности для кумил - и трет-бу-тилгидроперекисей, в литературе имеется не много. К - Рудиевского3, энергия димеризации rper - бутилгидроперекиси составляет 6 3 1 0 ккал / моль, а энергия присоединения каждой следующей молекулы 2 8 0 7 ккал / моль. [43]
Исследование ассоциации гидроперекисей должно помочь лучшему пониманию их физических и химических свойств. Однако соответствующих работ, в частности для кумил - и трет-бу-тилгидроперекисей, в литературе имеется не много. А: Беляев и Немцов2 криоскопическим путем для кумилгидропе-рекиси в бензоле и циклогексане при изменении моляльности в пределах 0 1 - 0 6 нашли, что величина f возрастает до 1 1 в первом и 1 8 во втором растворителе. По спектроскопическим данным В. В. Жаркова и Рудиевского3, энергия димеризации rper - бутилгидроперекиси составляет 6 3 1 0 ккал / моль, а энергия присоединения каждой следующей молекулы 2 8 0 7 ккал / моль. [44]
Страницы: 1 2 3