Бутилхлорид
Cтраница 3
Можно видеть, что mpem - бутилхлорид действительно отщепил хлорид-ион и протон. Несмотря на это, не совсем правильно говорят, что трет-бу-тилхлорид отщепляет хлористый водород. Поэтому элиминирование, при котором субстрат отщепляет протон и ион галогена, называют дегидрогало-генированием. [31]
При подобном же гидролизе mpem - бутилхлорида ( приведенного ниже) кинетические измерения показали, что скорость реакции зависит от концентрации галоидного соединения, но не зависит от концентрации гидроксильных ионов; реакция отвечает первому порядку и протекает с одинаковой скоростью в щелочном, нейтральном или кислом растворах. Таким образом, в этой реакции гидроксильный ион не участвует в элементарной, определяющей скорость реакции. [32]
Величина ACjf для сольволиза mpem - бутилхлорида также сильно зависит от состава растворителя. [33]
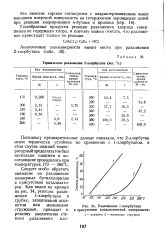 |
Разложение 1-хлорбутана в присутствии каталитической поверхности. [34] |
Следует особо обратить внимание на разложение изомерных бутилхлоридов в присутствии катализаторов. [35]
При взаимодействии этилена с erop - бутилхлоридом ожидаемый 1-хлор - З - метилпентан также не образуется. [36]
Бутилкаптакс получают по реакции бензотиазолтиола-2 с бутилхлоридом или бутилбромидом. [37]
Фотохимическое хлорирование бутана и других парафинов в бутилхлорид и алкилхлориды может быть осуществлено по Brooks y, EsSex y и Smith y49 таким образом, что смесь газообразных и жидких реагирующих веществ постепенно приближается к источнику освещения. Ayres 50 осуществил термическое хлорирование бутана и получил монохлорбутан ( другие парафины, содержащие больше двух углеродных атомов, также давали в основном моноклорированные продукты), смешивая пары углеводорода с недостаточным объемом хлора и нагревая смесь ( в отсутствии химически активного света, электрического разряда или катализатора) до температуры, достаточной для того, чтобы получить преимущественно монохлормро-ванные продукты и одновременно полностью использовать хлор. Было предложено также51 проводить хлорирование пропана или бутана до монохлорпроизвод-ных в паровой фазе в темноте, при температурах от 330 до 380 и вероятно в отсутствии катализаторов. Установлено, что основным продуктом является галоидный алкил и что реакции повидимому протекает мягко с полным использованием хлора ( или брома), присутствующего в реагирующих газах. Например реакция между бутаном и хлором в темноте ускоряется присутствием около 10 % бутилена. Однако, если1 вводить воздух или кислород в смесь насыщенных и ненасыщенных углеводородов, замещение несомненно замедляется, и происходит присоединение. [38]
Предложите метод рацемизации оптически активного emop - бутилхлорида, основываясь на том факте, что оптически активный emop - бутанол рацемизуется в разбавленной серной кислоте. [39]
Изотопный эффект в реакции сольволиза mpem - бутилхлорида, протекающей несомненно по диссоциативному механизму, близок по величине к эффекту в неводных средах. Примерно так же велики изотопные эффекты при сольволизе изопропиловых эфиров сульфокислот, механизм которого, как мы уже решили, носит также по существу SNl-характер. [40]
Кренцель и Н. А. Покотило [121] позволяют предложить метод получения бутилхлоридов газофазным гидрохлорированием бутиленов с применением в качестве катализатора природного алюмосиликата - асканита. [41]
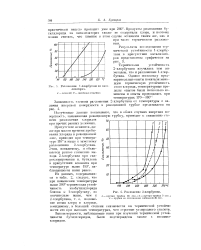 |
Разложение 2-хлорбутана. [42] |
Закономерности, наблюдаемые нами при изучении термической устойчивости бутилхлоридов, были подтверждены также с изоамил-хлоридом. [43]
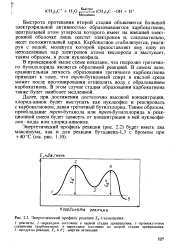 |
Энергетический профиль реакции SN 1-замещения. [44] |
В приведенной выше схеме показано, что гидролиз третичного бутилхлорида является обратимой реакцией. В самом деле, сравнительная легкость образования третичного карбокатиона приводит к тому, что трет-бутияоъъш спирт в кислой среде может после протонирования отщеплять воду с образованием карбокатиона. [45]
Страницы: 1 2 3 4