Статистическая поправка
Cтраница 1
Статистическая поправка, хотя и в неполном виде, была впервые предложена Бренстедом и Педерсеном [4], и позднее Бренстед [6] уточнил ее. Однако такая процедура не оправдана. [1]
Статистическая поправка не введена. [2]
Статистические поправки были применены при сравнении различных катализатооов между собой, а также при сравнении различных субстратов. [3]
Статистические поправки почти всегда делают для таких соединений, как дикарбоновые кислоты. Общепризнано также, что статистическую поправку необходимо делать для соединений, таких, как ион аммония, у которого один центр может служить поставщиком нескольких протонов. Однако большинство констант скоростей в литературе дано без учета такой возможности. Никаких поправок обычно не делают для атомов, имеющих несколько электронных пар, каждая из которых может акцептировать протон, таких, например, как анион кислорода. Статистические поправки обычно невелики, и эта проблема не имеет фундаментального значения для механизма кислотно-основного катализа. Данные, приведенные на рис. 4, не были исправлены на статистические эффекты, но даже если их ввести, то общее соответствие-точек прямой существенно не изменится. [4]
 |
Реакции гидратации-дегидратации при 25. [5] |
Эти статистические поправки не всегда учитывались, однако их введение не очень сильно влияет на результаты. Полученные таким образом данные приведены в табл. 3 и рассматриваются ниже для каждой индивидуальной реакции. [6]
Пг - статистическая поправка, учитывающая, что при монозамещении в монопроизводном бензола равноценны два орто -, два мета - и одно пара-положение, а в бензоле равноценны все шесть положений. [7]
Необходимость введения статистических поправок возникает, если сравнивают две кислоты, СО2Н ( СН2) пСОо ( I) - и СО2Н ( СО2) С02СНз ( II), где п опять-таки велико. С другой стороны, константа диссоциации кислоты ( I) будет в два раза меньше, чем кислоты ( II), поскольку сопряженное основание COJ ( СН2) СО2 обладает двумя эквивалентными группами, к которым может присоединяться протон, а основание СО2 ( СН2) ПСО2СН3 имеет только одно такое место. Очевидно, что непосредственное применение соотношения ( 105) приведет к ошибке. Чтобы получить правильный результат, необходимо умножить наблюдаемую константу диссоциации кислоты ( I) на 2, прежде чем подставлять ее в формулу Бренстеда. [8]
Если ввести статистическую поправку на различное число водородных атомов в первичных, вторичных и третичных аминах [197], можно рассматривать их совместно. [9]
Если не вводить статистических поправок, то точки для однозарядных анионов двухосновных карбоновых кислот будут значительно отклоняться от прямой линии, проведенной по точкам для анионов одноосновных кислот. Поправки следует вводить на том основании, что К. НООС ( СН2) СОО, так как эти ионы могут образовываться из кислоты НООС ( СН2) / Х) ОН двумя эквивалентными путями, а именно отщеплением протона от одной или от другой карбоксильной группы. [10]
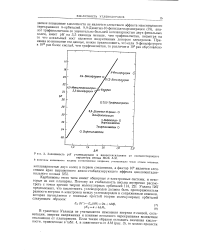 |
Зависимость рК углеводородов в циклогексиламине от соответствующего. [11] |
В величины кислотности введены статистические поправки, учитывающие число атомов водорода. [12]
Хотя в принципе метод статистических поправок теоретически обоснован, однако опытных данных, свидетельствующих о его пригодности, имеется мало. Атомы водорода находятся так близко друг к другу, что вероятность переноса протона при столкновении, повидимому, меньше учетверенной вероятности переноса в случае аналогичного иона, содержащего только один атом водорода. Однако само понятие аналогичного иона несколько туманно, поскольку в подобной системе невозможно заместить атомы водорода другой группой, не повлияв на природу оставшихся атомов водорода. Во-вторых, возникают трудности при выборе правильных величин q; эти трудности часто являются следствием того, что электронное строение изучаемых веществ однозначно не установлено. [13]
В константы должны быть внесены статистические поправки на количество эквивалентных протонов или мест для протонов в реагирующих веществах. [14]
СНз-группе составляет 4 2 после учета статистической поправки на число атомов водорода. Преимущественное образование более замещенного енола при катализируемой кислотой енолизации обычно объясняют стабилизующим эффектом алкильпых групп, находящихся при двойных углерод-углеродных связях. Противоположный стерический эффект, оказывающийся, по-видимому, значительным, наблюдается в случае 4 4-диметилпентанона - 2, где мегиле-новая группа, экранированная грег-бутильиой группой, становится менее реакционноспособной, чем метильная. Однако общее различие реакционной способности здесь значительно меньшее, чем при катализе образования енолятов основаниями. [15]
Страницы: 1 2 3