Порошок - кобальт
Cтраница 1
Порошок кобальта, присутствующий в реакционной массе при реакции Релена, является особенно активным. Однако альдольную конденсацию может вызвать также металл аппарата, в котором ведут процесс. [1]
Порошок кобальта поглощает от 50 до 100 объемов водорода и образует небольшое количество гидрида. [2]
Порошок кобальта и окись углерода под давлением 100 от при 200 реагируют с образованием карбонила кобальта Со2 ( СО) 8, который разлагается на воздухе при температурах выше 60 на кобальт и окись углерода. Мак-Кивер 14 ] описывает производство карбонила кобальта, основанное на приготовлении суспензии карбоната кобальта, основного карбоната кобальта и гидроокиси кобальта в нейтральной органической жидкости ( спирты или кетоны), которая является растворителем карбонила кобальта. [3]
 |
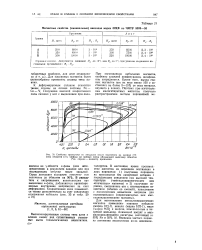
Производство альдегидов С7 - С9 по порошковой схеме оксосинтеза. [4] |
Часть порошка кобальта снова измельчается и возвращается в декобальтизер для увеличения поверхности, на которой отлагается выделяющийся при разложении карбонилов кобальт. [5]
Для изготовления металлокерамических магнитов применяют порошки кобальта ( марка КП-1), никеля ( марка НП-1), меди ( марка МП и железа, измельченные в вихревой мельнице. [7]
Другой метод состоит в нагревании порошка кобальта, смешанного с диэтиламингидрохло-ридом, до расплавленного состояния, охлаждении и измельчении образовавшейся массы, добавлении вновь полученного порошка к смеси циклопентадиена с диэтиламином, нагретой до 60 С, кипячении в течение 3 ч, промывке и фильтровании. Простым методом получения служит реакция между парами циклопентадиена, разбавленными азотом, и оксалатом кобальта в трубчатой печи86 при 370 - 375 С. [8]
Гетцель [8] сообщает о спекании порошка кобальта с железом, никелем, хромом, вольфрамом, молибденом, алюминием, бором и цинком. [9]
 |
Диаграмма. состояния псевдобинарной системы WC-Co. [10] |
Порошок карбида смешивают с соответствующим количеством мелкозернистого порошка кобальта, восстановленного из окиси. [11]
Порошок карбида смешивают с соответствующим количеством мелкозернистого порошка кобальта, восстановленного из закиси. [12]
В этом случае в реактор карбонилирования подается суспензия порошка кобальта в сырье, подготовляемая в специальной емкости. [13]
При нормальной температуре компактный кобальт стоек к действию воды и воздуха, хотя порошок кобальта на воздухе воспламеняется. Компактный кобальт начинает окисляться на воздухе выше 200 С, когда иа его поверхности образуется пленка смеси оксидов. Внутренний слой плотно пристает к кобальту и имеет зеленоватую окраску, внешний слой в виде налета черного цвета легко стирается. Кроме этих соединений с кислородом, известно соединение СоО - А12О3 синего цвета, так называемая тенарова синь. Это соединение может быть получено прокаливанием смеси СоО и АЬОз при температуре около 1000 С. [14]
Для изготовления сплавов третьей группы используют карбиды вольфрама, титана, тантала и порошок кобальта в качестве связки. Эти сплавы маркируют буквами ТТК и цифрами. Цифра, стоящая после букв ТТ указывает суммарное содержание карбидов титана TiC и тантала ТаС, а цифра, стоящая после буквы К - содержание кобальта. [15]
Страницы: 1 2 3