Порядок - активность
Cтраница 2
Из сопоставления данных, приведенных в табл. 67 - 69, видно, что порядок активностей катализаторов совпадает как для опытов в автоклавах, так, и в проточной установке. [16]
В основном влияние комплексообразования на реакционную способность ионов ртути [25] и серебра [12] допускает аналогичную интерпретацию, хотя необходимо отметить, что порядок активности различных комплексов отличается для всех трех металлов. Так, например, хлоридный и ацетатный комплексы иона ртути, обладающие большей стабильностью, чем соответствующие ионы комплекса Си2, менее реакционноспособны, чем водный комплекс, в то время как относительно нестабильный сульфатный комплекс является более реакционноспособным. В случае серебра, ацетатный и этилендиаминовый комплексы более реакционноспособны, чем некомплексный ион, в то время как очень стабильный цианидный комплекс неактивен. [17]
Эта чувствительная реакция на восстанавливающие сахара позволяет различать а-кетолы и простые альдегиды. Порядок активности участия в этой реакции следующий: фруктозаглюкозалактоза мальтозан-масляный альдегид. Реактив используется также для определения дегидрогеназы в тканях, клетках и бактериях, при изучении прорастания семян и для определения кортизона. [18]
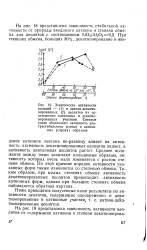
В более жестких условиях ( при - 140 - 190 С и давлении водорода примерно бОатм) смеси карбоксилатов металлов и триэтилалюминия ( соотношение алюминий: карбоксилат 3 или 4: 1) катализируют восстановление ароматических колец. Порядок активности металлов таков: никель кобальт железо хром медь. Другие соли металлов не так эффективны, как в реакции гидрирования олефинов. Введение алкильных групп в ароматическое кольцо уменьшает скорость гидрирования. Как и в случае олефинов, скорость гидрирования описывается уравнением - d [ Hz ] / dt k [ Hz ] [ катализатор ] и не зависит от концентрации субстрата. [19]
В более жестких условиях ( при - 140 - 190 С и давлении водорода примерно бОатм) смеси карбоксилатов металлов и триэтилалюминия ( соотношение алюминий: карбоксилат 3 или 4: 1) катализируют восстановление ароматических колец. Порядок активности металлов таков: никель кобальт железо хром медь. Другие соли металлов не так эффективны, как в реакции гидрирования олефинов. Введение алкильных групп в ароматическое кольцо уменьшает скорость гидрирования. Как и в случае олефинов, скорость гидрирования описывается уравнением - d [ H2 ] / dt k [ H. [20]
При этом предполагается, что в значениях энтропии активации нет существенных различий - вполне вероятное допущение для стерически незатрудненных мономеров. Этот порядок активности представляет в общем виде данные табл. 6.3 и 6.4 и многие данные по гомополимеризации. [21]
Влияние заместителя на активность мономеров при катионной сополимеризации зависит от того, в какой степени этот заместитель увеличивает электронную плотность двойной связи, и от его способности к резонансной стабилизации образующегося иона карбония. Однако порядок активности мономеров при катионной сополимеризации ( так же, как и при анионной) далеко не так легко установить, как при радикальной сополимеризации. На активность мономера часто более сильно влияют условия реакции, чем строение мономера. [22]
Скорости гидрогенолиза неопентана в присутствии нанесенных Rh -, Ru -, Pd -, Os -, Ir -, Pt -, Си - и Аи-катализаторов при 250 C, отнесенные к единице поверхности металла, сильно отличаются друг от друга, в ряде случаев в 100 раз; наиболее активным является Ru-катализатор, наименее активным - Аи. При этом порядок активности коррелируется со степенью заполнения d - уровня металла. Среди исследованных металлов VIII группы, а также Си и Аи, лишь Ir, Pt и Аи активны в реакции изомеризации неопентана в изопентан, что, по мнению авторов [34], обусловлено высокой электроотрицательностью этих металлов. [23]
При сопоставлении активности катализаторов в реакциях электроокисления возникают трудности, вызванные тем, что наклон тафелевских зависимостей различен на разных электродах. Таким образом, порядок активности зависит от интервала потенциалов, в котором производится сравнение. [24]
Среднее положение между ними занимают кальциевые образцы, активность которых очень мало изменяется с ростом степени обмена. По этой причине порядок активности указанных форм также изменяется со степенью обмена. Таким образом, при малых степенях обмена активность декатионированных цеолитов превосходит активность катионных форм, однако при больших степенях обмена наблюдается обратная картина. [26]
На обоих носителях найден следующий порядок изменения каталитической активности металлов в реакции гидрогенизации бензола: RuPt PdTcRe. Предполагается, что такой порядок активностей связан со способностью этих металлов хемосорбировать водород при комнатной температуре, которая изменяется в том же порядке. [27]
Видно, что для индивидуальных газов СО и С2Н4 наиболее активными оказались окись кобальта и медно-хромовый катализатор. При окислении смеси газов порядок активности катализаторов изменяется. [28]
Эта реакция осуществляется под давлением и ускоряется различными катализаторами ( стр. Оказывается, что те же катализаторы сохраняют порядок активности и при разложении метанола ( при нормальном давлении), чем широко пользовались различные исследователи при подыскании активных катализаторов для синтеза под давлением. [29]
Индивидуальные хиноциклины А и В имеют тот же порядок активности в отношении грамположительных бактерий, что и неразделенный комплекс, но они значительно активнее в отношении патогенных кислотоустойчивых бактерий. Изохиноциклины А и В менее активны, чем комплекс, в отношении грамположительных и непатогенных кислотоустойчивых бактерий, но они подавляют патогенные кислотоустойчивые микроорганизмы при том же порядке концентрации. Острая токсичность хиноциклинового комплекса невелика ( мыши переносят per os до 400 мг / кг), однако при повторном его введении он проявляет высокую токсичность. [30]
Страницы: 1 2 3