Истинный порядок - реакция
Cтраница 1
Истинный порядок реакции п в этом случае получается равным нулю. [1]
 |
Зависимость lg W oilg [ MJ Рис - Зависимость скоростей ( 1 и 2 и lg W от lg ( [ М ] - [ М ] ( 3. обратимой полимеризации от кон. [2] |
Отсюда истинный порядок реакции по мономеру - первый. [3]
Для установления истинного порядка реакции весьма важно вести измерения настолько долго, насколько это возможно. Однако для каталитических процессов это условие не всегда легко выполнить, так как одни катализаторы становятся активными лишь после некоторого индукционного периода, другие же, наоборот, с течением времени разлагаются. Следует иметь в виду, что для получения надежных кинетических данных необходимо очень тщательнэе исследование каталитического процесса, так как в противном случае полученные результаты не будут иметь никакой научной ценности. [4]
Задача установления истинного порядка реакций углерода с газами осложняется, если на скорость газификации влияет торможение продуктами реакции и скорость переноса реагирующих веществ к поверхности твердого тела. Торможение продуктами реакции может приводить к более низким порядкам реакции, в то время как торможение, обусловленное переносом, повышает или понижает кажущийся порядок в зависимости от истинного порядка реакции и природы фактора, регулирующего процесс переноса вещества. В разделах V и VI эти усложняющие факторы будут обсуждены более подробно. Остальная часть этого раздела посвящена исследованиям порядка реакций углерода с газами. [5]
Для гетерогенных реакций истинный порядок реакции не всегда совпадает с определенным или кажущимся. [6]
 |
Зависимость степени гидролиза и-ксилилендихлорида в среде 80 % - ного спирта при 75 С ( а и в водной среде при 80 С ( б от мольного соотношения С6Н4 ( СН2С1 2. NaOH. [7] |
Таким образом, истинный порядок реакции гидролиза п-ксилилендихлорида второй, но он может быть первым или нулевым в зависимости от условий реакции. [8]
В связи с этим истинный порядок реакции может е совпадать с описанным выше формальным ( по сумме стехиометрических коэффициентов) и быть даже дробным. [9]
Выразите эти данные в виде графика в соответствии с интегральной формой уравнения скорости реакции второго порядка и найдите истинный порядок реакции. [10]
Мы получаем, таким образом, из экспериментальных данных Паркера и Хот-теля свидетельство в пользу того, что истинный порядок реакции углерода с кислородом значительно ниже единицы. [11]
 |
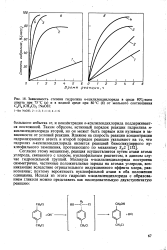
Зависимость кинетики броми.| Скорость бромировашш бензола. [12] |
Такое явление может наблюдаться, если реакция тормозится какими-нибудь продуктами реакции, в нашем случае монобромбензолом, что и соответствует повышению истинного порядка реакции благодаря тому, что в концентрационное уравнение вместо [ ZnBr2 ] входит множитель [ катализатор ] ( 1 - Кх), где К - константа равновесия для образования и распада тормозящего комплекса и х - концентрация монобромбензола. [13]
Такой дробный порядок является кажущимся. Истинный порядок реакции, протекающей на поверхности катализатора, является первым. Кажущийся порядок получаем потому, что в кинетическое уравнение согласно принятому нами методу расчета вводим величины, характеризующие изменение концентрации вещества не непосредственно на поверхности, а в объеме. Поверхностная концентрация, которая пропорциональна величине 6, входит в уравнение кинетики ( XII, 81) в первой степени и, следовательно, истинный порядок реакции - первый. Примером реакции с дробным кажущимся порядком является реакция распада аммиака на мышьяке. [14]
Такой дробный порядок является кажущимся. Истинный порядок реакции, протекающей на поверхности катализатора, является первым. Кажущийся порядок получаем потому, что в кинетическое уравнение, согласно принятому нами методу расчета, вводим величины, характеризующие изменение концентрации вещества не непосредственно на поверхности, а в объеме. Поверхностная концентрация, которая пропорциональна величине 0, входит в уравнение кинетики ( XII, 81) в первой степени и, следовательно, истинный порядок реакции - первый. Примером реакции с дробным кажущимся порядком является реакция распада аммиака на мышьяке. [15]
Страницы: 1 2 3