Истинный порядок - реакция
Cтраница 2
Экспериментальные результаты показывают, что реакции в смесях, богатых этиленом, никогда не подчиняются тому кинетическому закону, который был установлен для других смесей. При 162 С истинный порядок реакции может быть определен только для смесей, богатых водородом. [16]
Известно, что для реакции углерода с кислородом легко наблюдалась чисто диффузионная область без малейшего следа каких-либо искажений, связанных с истинной кинетикой на поверхности. Это объясняется именно тем, что истинный порядок реакции ниже первого и может служить лишним доводом в пользу последнего заключения. [17]
Как видно из последнего, увеличение концентрации трег-бутилхлорида при наличии малой добавки этанола в качестве электрофильного агента в нитробензоле приводит к постепенному уменьшению наблюдаемой константы скорости сольволиза вплоть до значений, характерных для смесей трет-бутл-хлорида с нитробензолом без каких-либо добавок. Такая картина не могла бы наблюдаться, если бы истинный порядок реакции по этанолу был равен единице. [18]
Величина в, входящая в ( XX. Ввиду того что скорость реакции содержит в в первой степени, истинный порядок реакции всегда равен единице. Кажущийся порядок этой реакции связан с зависимостью скорости реакции от концентрации ( или давления) внутри газовой фазы, и, как видно из ( XX. [19]
Таким образом, для вычисления п нужно знать скорость данной реакции при двух концентрациях исходного вещества. Если каждая из этих концентраций отвечает началу реакции, то определяется истинный порядок реакции; если С и Ci соответствуют различным моментам времени в ходе продолжающейся реакции, то получается иное значение п ( временной порядок) вследствие влияния на скорость реакции образующихся продуктов. [20]
Таким образом, для вычисления п нужно знать скорость данной реакции при двух концентрациях исходного вещества. Если каждая из этих концентраций отвечает началу реакции, то определяется истинный порядок реакции; если Ci и с соответствуют различным моментам времени в ходе продолжающейся реакции, то получается иное значение п ( временной порядок) вследствие влияния на скорость реакции образующихся продуктов. [21]
Величина в, входящая в ( XX. Ввиду того что скорость реакции содержит в в первой степени, истинный порядок реакции всегда равен единице. Кажущийся порядок этой реакции связан с зависимостью скорости реакции от концентрации ( или давления) внутри газовой фазы, и, как видно из ( XX. [22]
При любом радиусе г скорость реакции, отнесенная к единице поверхности, может быть рассчитана из коэффициента ( dn / dt) r / Sr. Следовательно, нанесение на график удельной скорости реакции и рассчитанной концентрации двуокиси углерода при одном и том же значении г дает возможность определить истинный порядок реакции, не осложненный диффузией. Из вспомогательного графика, аналогичного рис. 19, была определена конечная скорость реакции при нулевой концентрации двуокиси углерода. [23]
Задача установления истинного порядка реакций углерода с газами осложняется, если на скорость газификации влияет торможение продуктами реакции и скорость переноса реагирующих веществ к поверхности твердого тела. Торможение продуктами реакции может приводить к более низким порядкам реакции, в то время как торможение, обусловленное переносом, повышает или понижает кажущийся порядок в зависимости от истинного порядка реакции и природы фактора, регулирующего процесс переноса вещества. В разделах V и VI эти усложняющие факторы будут обсуждены более подробно. Остальная часть этого раздела посвящена исследованиям порядка реакций углерода с газами. [24]
Правильное представление об истинном порядке реакций углерода с газами осложняется тогда, когда на скорость газификации оказывают влияние продукты реакции, обладающие тормозящим воздействием, и скорость переноса вещества реагентов к поверхности твердого тела. Торможение продуктами реакции может дать в результате слишком низкий порядок реакции, в то время как торможение переносом вещества может или повысить, или понизить кажущийся порядок в зависимости от истинного порядка реакции и закономерностей переноса вещества. Ниже в этом разделе будут даны ссылки, где можно получить сведения о порядке реакции углерода с газами. [25]
Время, требующееся для того, чтобы израсходовалась заданная часть, скажем половина, одного из исходных веществ, при различных порядках реакции зависит от первоначальной концентрации реагентов различным образом. Если проведено несколько экспериментов с сильно различающимися исходными концентрациями реагентов, то, сравнивая значения времени полупревращения ( или времени превращения какой-либо иной части, более соответствующей имеющимся экспериментальным данным) в различных экспериментах, можно определить истинный порядок реакции. [26]
Время, требующееся для того, чтобы израсходовалась заданная часть, скажем полоэина, одного из исходных веществ, при различных порядках реакции зависит от первоначальной концентрации реагентов различным образом. Если проведено несколько экспериментов с сильно различающимися исходными концентрациями реагентов, то, сравнивая значения времени полупревращения ( или времени превращения какой-либо иной части, более соответствующей имеющимся экспериментальным данным) в различных экспериментах, можно определить истинный порядок реакции. [27]
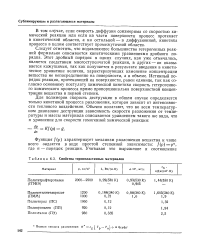 |
Свойства термопластичных материалов. [28] |
Следует отметить, что подавляющее большинство гетерогенных реакций формально описывается кинетическими уравнениями дробного порядка. Этот дробный порядок в одних случаях, как уже отмечалось, является следствием многоступенчатой реакции, в других - он оказывается кажущимся, так как получается в результате введения в кинетическое уравнение величин, характеризующих изменение концентрации вещества не непосредственно на поверхности, а в объеме. Истинный порядок реакции, протекающей на поверхности, равен единице, так как согласно основному постулату химической кинетики скорость гетерогенного химического процесса прямо пропорциональна поверхностной концентрации вещества в первой степени. [29]
Как видно, порядок такой реакции получается дробным. Такой дробный порядок является кажущимся. Истинный порядок реакции, протекающий на поверхности катализатора, является первым. Кажущийся порядок мы получаем потому, что в уравнение кинетики, согласно принятому нами методу расчета, входят величины, характеризующие изменение концентрации вещества не непосредственно на поверхности, а в объеме. Поверхностная концентрация, которая прямо пропорциональна величине о, в ходит в уравнение кинетики ( 132) в первой степени, и, следовательно, истинный порядок реакции первый. Примером реакции с дробным кажущимся порядком является реакция распада аммиака на мышьяке. [30]
Страницы: 1 2 3