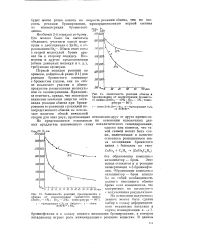
Первый порядок - реакция
Cтраница 1
Первый порядок реакции можно получить, считая реакцию ( 1) бимолекулярной, что весьма вероятно. Однако значение энергии активации совершенно неприемлемо, следовательно, реакция ( 2) не может быть стадией цепного процесса. [1]
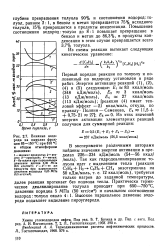 |
Влияние водорода на пиролиз фракции 85 - 150 С при 810 С и общем атмосферном давлении. [2] |
Первый порядок реакции по толуолу и половинный по водороду установлен в ряде работ. [3]
Первый порядок реакции, независимость скорости от концентрации нуклеофила, постоянство константы скорости при переходе от Н2О к D2O, указывают, что нуклеофил, в частности вода, не участвует в стадии, определяющей скорость реакции, и противоречит предположению о механизме присоединения-отщепления; отсутствие же обмена водорода на дейтерий в среде D2O исключает промежуточное образование арина. [4]
Первый порядок реакции по одному из реагентов и нулевой по другому свидетельствуют о предварительной диссоциации этого реагента, которая обычно происходит медленно и потому определяет итоговую кинетику реакции. В этом случае часто наступает рацемизация, конечно, если речь идет о замещении у асимметрического тетраэдрического углерода. В переходном состоянии в этом случае участвует частица диссоциированной молекулы ( ион) и молекула второго реагента. [5]
Первый порядок реакции наблюдается также по активности - ОН. [6]
Первый порядок реакции по времени найденный ранее [11] для реакции бромистого алюминия с бромистым этилом, сам по себе не исключает участия в обмене продуктов расщепления молекулы или ее полимеризации. Приходится отметить, правда, что некоторое снижение значения энергии активации реакции обмена при броми-ровании в сравнении с реакцией непосредственного обмена не исключает наличия общей начальной стадии для этих двух, протекающих независимо друг от друга процессов. [8]
Первый порядок реакции по отношению к NO в этом случае может быть обусловлен медленной адсорбцией окиси азота на поверхности катализатора. Такое предположение выдвинуто Винтером [280], исследовавшим разложение NO на сорока различных окислах в области температур 330 - 870 С. [9]
Первый порядок реакции, независимость скорости От концентрации нуклеофила, постоянство константы скорости при переходе от HgO к D2O указывают, что нуклеофил, в частности вода, не участвует в стадии, определяющей скорость реакции, и противоречат предположению о механизме присоединения - отщепления, а отсутствие обмена водорода на дейтерий в среде ТЬО исключает промежуточное образование арина. Малая селективность по отношению к нуклеофилам свидетельствует о высокой vактивности промежуточной частицы - арил-катиона [341], стадия генерирования которого определяет скорость все-то процесса. [10]
Первый порядок реакции ftO мономеру имеет место при мультимолекулярной адсорбции мономера, завышенный порядок реакции - при менее чем монослойной адсорбции. [11]
Первый порядок реакции димеризации может быть обусловлен тем, что скорость самой реакции превосходит скорость процесса активации, происходящего в самой молекуле. Такое объяснение неминуемо должно было бы требовать, чтобы природа активации молекул, образующих димер, и молекул, образующих полимер, была бы различна, а также и различны должны были бы быть и скорости активации, иначе нельзя было бы объяснить второй порядок реакции полимеризации. [12]
Первый порядок реакции димеризации может быть обусловлен тем, что скорость самой реакции превосходит скорость процесса активации, происходящего в самой молекуле. Такое объяснение неминуемо должно было бы требовать, чтобы природа активации молекул, образующих димер, и молекул, образующих полимер, была бы различна, а также и различны должны были бы быть и скорости активации, иначе нельзя было бы объяснить второй порядок реакции полимеризации. [13]
Допускаем первый порядок реакции в обоих направлениях, считаем, что в самом начале система состояла только из вещества В, и поэтому концентрации В и С пропорциональны соответственно 1 - и, где, как и прежде, степень полноты реакции - химическая переменная. [14]
Выявлен первый порядок реакции по сероводороду и установлено ускоряющее влияние водорода и окиси углерода на извлечение сероводорода из газов. [15]
Страницы: 1 2 3 4