Первый порядок - реакция
Cтраница 3
Это указывает на первый порядок реакции образования грег-бутилперацетата по гидроперекиси и по уксусному ангидриду. [31]
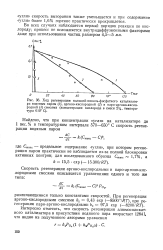 |
Ход регенерации кальций-никель-фосфатного катализатора водяным паром ( /, аргоно-кислородной ( 2 и паро-аргоно-кисло-родной ( 3 смесями ( концентрация кислорода в смеси 2 %, температура 610 С. [32] |
Во всех случаях наблюдается первый порядок реакции по кислороду; процесс не осложняется внутридиффузионными факторами даже при использовании частиц размером 4 5 - 5 мм. [33]
Таким образом был установлен первый порядок реакции по каждому из ее компонентов. [34]
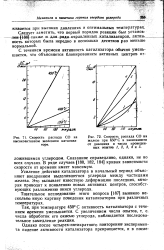 |
Скорость распада СО на высокоактивном железном катализаторе.| Скорость распада СО на железе при 650 С в зависимости от давления и числа проведенных опытов /, 2, 3, 4 я 5. [35] |
Следует заметить, что первый порядок реакции был установлен [188] также дд - яда-травденшлх катализаторов актив ность которых была нередко в несколько десятков раз меньше нормальной. [36]
Данные табл. VI.13 подтверждают первый порядок реакции изомеризации, поскольку селективность ни одного из процессов не зависит от парциального давления: в серии М-1 были получены одинаковые селективности при введении окиси бутена-1 и г / шг-бутена-2, независимо от того, являлось ли вещество основным1 неактивным компонентом или примесным, радиоактивным, парциальное давление которого в импульсе было-на три порядка меньше нерадиоактивного. Такие же результаты были получены в серии М-2, когда парциальные давления реагирующих веществ были одинаковыми. [37]
Для всех случаев катализа установлен первый порядок реакции по катализатору и сложный по гидроперекиси. Предложены схема и возможный механизм процесса, рассчитаны основные кинетические константы. [38]
В ряде работ был подтвержден первый порядок реакции при пониженных и повышенных по сравнению с данными [116] значениями энергии активации и предэкспоненциалыгого члена, что можно объяснить использованием технического дихлорэтана с разной комбинацией и концентрацией примесей, а также неодинаковым состоянием стенок реактора. [39]
Вместе с тем обычно обнаруживаемый первый порядок реакции по отношению к водороду указывает на возможность того, что водород приближается к ненасыщенному ядру из реакционного пространства, со стороны, противоположной катализатору. [40]
Для всех случаев катализа установлен первый порядок реакции по катализатору и сложный по гидроперекиси. Предложены схема и возможный механизм процесса, рассчитаны основные кинетические константы. [41]
Экспериментально подтвержденный большинство исследователей факт первого порядка реакции С С02 ( и не только этой реакции) еще не означает, что она протекает посредством прямого реагирования молекул СО 2 с углеродом, как это принимается в формальной кинетике. Подобные этому явления обусловливаются, очевидно, тем, что стадия, определяющая скорость реакции, протекает по первому порядку. Таковой в реакции С С02 является, очевидно, стадия ударного распада промежуточного углерод-кислородного комплекса. [42]
Цухановой, кроме косвенной проверки первого порядка реакции, предположенного в граничном условии, произведено еще прямое исследование его в опытах с изменением концентрации, Полученная линейная зависимость вполне оправдывает первый порядок реакции. [43]
Следует иметь в виду, что первый порядок реакции еще не свидетельствует об обязательной мономолекулярности процесса. [44]
При 90 С мы имеем достаточно четко выраженный первый порядок реакции. [45]
Страницы: 1 2 3 4