Суммарный порядок - реакция
Cтраница 1
Суммарный порядок реакции, идущей в одну стадию, не может быть больше трех; реакции с участием большего числа частиц не наблюдались. [1]
Суммарный порядок реакции взаимодействия перекиси с аминами, согласно схеме, зависит от того, какая из реакций обрыва или передачи цепи доминирует и какова относительная активность возникших в результате элементарных актов свободных радикалов. [2]
Видно, что суммарный порядок реакции равен нулю, порядок реакции по отношению к продукту равен - 1, и скорость реакции уменьшается с увеличением концентрации продуктов реакции. Этот результат следует из того, что при сильной адсорбции продуктов реакции они занимают почти все центры адсорбции, тем самым препятствуя адсорбированию реагента. [3]
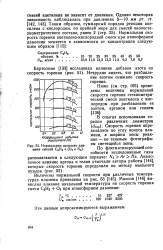 |
Нормальная скорость пла - ям светящейся ЗОНЫ. [4] |
Таким образом, суммарный порядок реакции ацетилена с кислородом, по крайней мере для смесей околосте-хиометрического состава, равен 2 ( стр. [5]
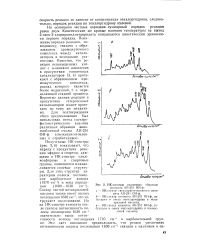 |
ИК-спсктры различных образцов. [6] |
На основании частных порядков суммарный порядок реакции равен двум. Кинетические же кривые влияния температуры на выход 2-окси - З - хлорпропилметакрилата описываются кинетическим уравнением первого порядка. Понижение порядка реакции, по-видимому, связано с образованием промежуточного комплекса между катализатором и исходными реагентами. Вероятно данная реакция в присутствии гетерогенных катализаторов может протекать по тому же механизму. [7]
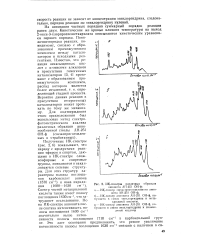 |
ИК-спектры различных образцов. [8] |
На основании частных порядков суммарный порядок реакции равен двум. Кинетические же кривые влияния температуры на выход 2-окси - З - хлорпропилметакрилата описываются кинетическим уравнением первого порядка. Понижение порядка p - еакции, по-видимому, связано с образованием промежуточного комплекса между катализатором и исходными реагентами. Вероятно данная реакция в присутствии гетерогенных катализаторов может протекать по тому же механизму. [9]
Уравнение ( IV-1) позволяет установить суммарный порядок реакции при различных условиях эксперимента. Когда выход окиси углерода мал Pco-Cl, порядок реакции по двуокиси углерода может быть первым или нулевым в зависимости от того, будет ли член kspco, значительно меньше или значительно больше единицы. Если по условиям опыта нельзя пренебречь ни одним из членов уравнения ( IV-1), порядок реакции может оказаться и дробным. [10]
Изменение температуры может вызывать и изменение суммарного порядка реакции. [11]
При этом порядок по отдельному компоненту и суммарный порядок реакции всегда являются целыми положительными числами. Для отдельной стадии процесса порядок обычно не превышает трех. В соответствии с этим особо важное значение в химической кинетике имеют реакции первого, второго и третьего порядков. [12]
При окислении сероводорода на алюмооксидном катализаторе наблюдается полуторный суммарный порядок реакции. Исходя из предположения, что порядок реакции по кислороду составляет обычно величину, близкую к 0 5, можно сделать вывод о первом порядке по сероводороду для исследованного катализатора. [13]
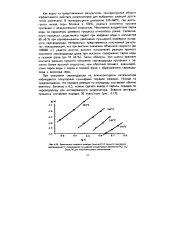 |
Зависимость скорости реакции ( ммоль / ( ст прямого окисления. [14] |
При окислении сероводорода на алюмооксидном катализаторе наблюдается полуторный суммарный порядок реакции. Исходя из предположения, что порядок реакции по кислороду составляет обычно величину, близкую к 0 5, можно сделать вывод о первом порядке по сероводороду для исследованного катализатора. [15]
Страницы: 1 2 3 4