Суммарный порядок - реакция
Cтраница 3
Такая реакция является реакцией второго порядка по отношению к реагенту А и первого порядка по отношению к реагенту В, суммарный порядок реакции является третьим. [31]
Полученная зависимость в координатах lg Wj [ ДХДФС ] представляет собой уравнение прямой линии, тангенс угла наклона которой соответствует величине суммарного порядка реакции. Однако построение этой зависимости по экспериментальным данным ( рис. 2) показало, что суммарный порядок реакции непрерывно возрастает по мере протекания процесса. Это можно объяснить ингибирующим действием образующегося в реакции хлористого натрия ( рис. 3), которое, по-видимому, является проявлением эффекта одноименного иона. [32]
Полученные данные свидетельствуют о том, что при постоянной температуре нормальная скорость пламени распада ацетилена не снижается с ростом давления, следовательно суммарный порядок реакции не может быть меньше второго. [33]
Проведенными исследованиями [4.10] установлено, что при постоянной температуре нормальная скорость пламени распада ацетилена не снижается с ростом давления, следовательно, суммарный порядок реакции не может быть меньше второго. [34]
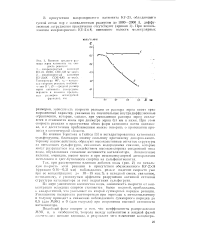 |
Влияние среднего pa. i-мера зерня катионита на скорость реакции. [35] |
По мере увеличения количества воды, зависимость скорости от концентрации исходных спиртов становится более пологой, приближаясь к квадратичной, что указывает на второй суммарный порядок реакции. [36]
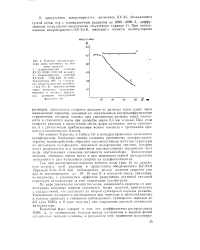 |
Влияние среднего размера зерна катионита на скорость реакции. [37] |
По мере увеличения количества воды, зависимость скорости от концентрации исходных спиртов становится более пологой, приближаясь к квадратичной, что указывает на второй суммарный порядок реакции. Уменьшение полярности растворителя при переходе к метилэтилкетону и толуолу приводит к снижению наблюдаемого суммарного порядка до 0 5 ( для МЭК) и 0 ( для толуола) при сохранении высокой активности катализатора. [38]
Полученная зависимость в координатах lg W j 1д [ ДХДФС ] j представляет собой уравнение прямой линии, тангенс угла наклона которой соответствует величине суммарного порядка реакции. Однако построение этой зависимости по экспериментальным данным ( рис. 2) показало, что суммарный порядок реакции непрерывно возрастает по мере протекания процесса. Это можно объяснить ингибирующим действием образующегося в реакции хлористого натрия ( рис. 3), которое, по-видимому, является проявлением эффекта одноименного иона. [39]
Угловой коэффициент наклона прямой линии, изображающей эту зависимость для серии кинетических кривых, отвечающих разным [ Ai ] o, дает непосредственно величину суммарного порядка реакции. [40]
К сожалению, данные Глика также не дают возможности надежно определить кинетическое уравнение термического разложения окиси азота, так как в работе [3] не установлен суммарный порядок реакции и зависимость скорости реакции от концентраций отдельных компонентов в широком диапазоне их изменения, а обработка данных проводилась в предположении обратимого бимолекулярного процесса. Весьма возможно, что при другом способе обработки данных значение константы скорости и вид кинетического уравнения могут измениться. [41]
Тогда легко видеть, что если, например, скорость прямой реакции в 10 раз превышает скорость обратной ( при всех допустимых значениях с и cz) и если суммарный порядок реакции находится в пределах от 1 до 4, то функция достижимости вогнута по с и оптимальным будет переключательный режим по скорости потока и концентрации подаваемого сырья. [42]
 |
Схема перехода от изотермической автокаталитической реакции к цепочно-тепловому взрыву. [43] |
При чисто тепловом механизме самовоспламенения связь между логарифмами периода индукции и давления должна быть линейной, а угловой коэффициент этой прямой, равный ( / - s), будет определять суммарный порядок реакции. Линейно должен зависеть Igr и от 1 / Г0; угловой коэффициент этой прямой ( с учетом поправки 2sRT0) будет определять эффективную энергию активации. [44]
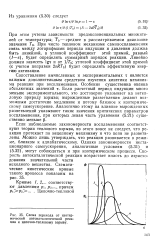 |
Схема перехода от изотермической автокаталитической реакции к цепочно-тепловому взрыву. [45] |
Страницы: 1 2 3 4