Кинетический порядок - реакция
Cтраница 1
Кинетический порядок реакции по данному реагенту определяется путем изменения концентрации только этого реагента и оценки влияния такого изменения на суммарную скорость реакции. Например, если при повышении концентрации данного соединения вдвое скорость увеличивается в 2 раза, то это реакция первого порядка ( 21) по данному реагенту. Если при увеличении концентрации вдвое скорость реакции увеличивается в 4 раза, то это реакция второго порядка ( 22) по этому реагенту. [1]
Кинетический порядок реакции зависит от доминирующего состояния агрегации соли [450]: свободные ионы вступают в реакции, имеющие второй порядок, ионные пары - первый порядок, ионные тройники - порядок две третьих, ионные квадруполи - порядок одна вторая. [2]
Кинетический порядок реакции зависит от условий, существующих на поверхности сосуда, но скорость реакции всегда убывает с ростом температуры. Значит, реакция идет через образование малостойкого при повышенной температуре промежуточного продукта, а не путем непосредственного соединения компонентов. [3]
Кинетический порядок реакции относительно реактива R не имеет существенного значения, поскольку концентрация R остается постоянной во всех опытах. [4]
Кинетический порядок реакции может быть выражен не целым числом. [5]
Кинетический порядок реакции распада также зависит от растворителя. [6]
Кинетический порядок реакции крекинга парафиновых углеводородов во многих случаях несколько отклоняется от первого и находится в зависимости от начального давления углеводорода и глубины превращения его. Это обстоятельство осложняет задачу определения констант скорости крекинга углеводородов и увеличивает число необходимых опытов. [7]
Для определения кинетического порядка реакции крекинга необходимо провести серию опытов крекинга при одной и той же температуре, но при различных начальных концентрациях углеводородов. [8]
Что касается кинетического порядка реакции гидрирования в присутствии MoS2, то на примере толуола при 420 Альтман и Немцов [2] показали, что по углеводороду реакция имеет порядок, близкий к нулевому, а по водороду - первый порядок. Энергия активации достигает значительной величины, незакономерно колеблясь-в интервале 400 - 460 от 19800 до 26900 кал. [9]
Яз я - общий кинетический порядок реакции; ni, П2, Пз - порядок реакции по отношению к веществам А, В, С; / ii, nz, Пз могут быть целыми или дробными числами. Реакции, скорость которых постоянна и не зависит от концентрации реагирующих веществ, имеют нулевой порядок. [10]
Обычно невозможно установить кинетический порядок реакций сольволиза относительно растворителя, так как растворитель присутствует в большом избытке. Заключение, по какому из этих или иных механизмов идет данная аллиль-ная сольволитическая реакция, должно базироваться на косвенном доказательстве. [11]
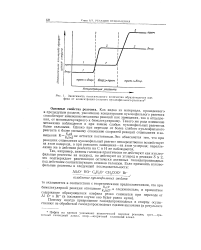 |
Зависимость относительного количества образующегося оле-фина от концентрации сильного нуклеофильного реагента. [12] |
Цифры на кривых указывают кинетический порядок реакции; трет. [13]
Близкий к нулю ( кинетический порядок реакции по SnCb указывает на то, что, по-видимому - - процесс лимитируется распадом промежуточного комплекса Sn2 с С2, концентрация которого определяется максимально возможной растворимостью iO2 и е зав-исит от концентрации холОр истого олова ( ряс. [14]
Выражение для скорости дает кинетический порядок реакции. Данная реакция имеет второй порядок, так как первая часть равенства содержит произведение двух концентраций. Реакция имеет первый порядок по водороду, поскольку [ Нз ] входит в уравнение в первой степени. [15]
Страницы: 1 2 3 4