Кинетический порядок - реакция
Cтраница 3
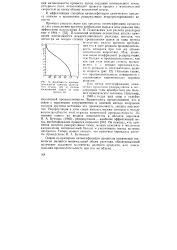 |
Зависимость производительности единицы реакторного объема ( G от степени превращения сырья за один проход ( х. [31] |
Показано также, что производительность повышается с увеличением кинетического порядка реакции. [32]
Рассмотрим кратко закономерности развития реакций во времени, когда стехиометрический и кинетический порядок реакции совпадают и равны единице, двум и трем. Наиболее часто встречаются реакции первого и второго порядка. Реакции других порядков сравнительно редки. [33]
Влияние заместителей свидетельствует о нуклеофильном характере замещения атомом серы, а первый кинетический порядок реакции и отсутствие обмена арильными группами при перегруппировке несимметричных тиокарбонатов ArO-CS-ОАгг или смесей О-арилтиокарбаматов, содержащих разные арильные группы-о внутримолекулярном характере реакций. [34]
Хотя эти изменения в ряде случаев можно обнаружить и с помощью измерения кинетического порядка реакции, однако это удается сделать далеко не всегда. К тому же многие реакции часто целесообразно проводить по псевдопервому порядку, что исключает возможность кинетической регистрации изменения механизма. [35]
В выражении для скорости концентрация КОН дана в первой степени; говорят, что кинетический порядок реакции равен 1 по отношению к КОН или что эта реакция первого порядка относительно КОН. [36]
Если в выражении для скорости концентрация КОН дана в первой степени, считают, что кинетический порядок реакции равен 1 по отношению к КОН или что эта реакция первого порядка относительно КОН. [37]
Здесь введена новая константа k k pf р, a n р q г - общий кинетический порядок реакции. Уравнение (2.74) приведено к виду (2.62), в связи с чем вновь становится применимым обсуждаемый метод полупревращения. Имеется, впрочем, важное ограничение использования последнего варианта. Он исключает изучение влияния продуктов на скорость, так как их концентрация не может в ходе опыта оставаться пропорциональной концентрации исходного вещества. [38]
Этот механизм может объяснить ряд явлений, таких, как эффект растворителя и добавляемых анионов на скорости и кинетический порядок реакции. Так, протон и ион металла будут стабилизироваться в разной степени растворителем или анионами. Конкуренция этих стабилизированных форм за СиН определяет наблюдаемые явления. [39]
Поскольку обозначения предназначены для отличия механизмов реакции, молекулярность реакции играет первостепенную роль, в то время как кинетический порядок реакции представляет собой только одну из измеримых количественных ее характеристик и зависит частично от механизма реакции, а частично от факторов, не связанных с механизмом. При применении понятия молекулярности для номенклатуры и обозначения механизма реакции следует иметь в виду следующие обстоятельства. Сложную реакцию можно условно характеризовать молекулярностъю стадии, определяющей скорость реакции. Молекулярность той или иной стадии реакции представляет собой число молекул, в которых обязательно происходят изменения ковалентности связей. Этому определению, используемому с 1933 г. [12] и прочно вошедшему в обиход, надо отдать предпочтение перед определением, основанным на числе всех молекул, принимающих участие в реакции или вступающих в реакцию. Несмотря на то что необходимость в такой трактовке в свое время специально подчеркивалась [18], в некоторых работах [19] она не была учтена; поэтому хотелось бы еще раз отметить роль молекулярности для того, чтобы данное нами определение было достаточно общим и пригодным для реакций в растворе. Обычно в подобных реакциях, в большей или меньшей степени, участвует неизвестное число молекул растворителя, особенно молекул полярного растворителя, а иногда и полярные молекулы растворенного вещества. Эти молекулы оказывают электростатическое влияние на взаимодействующие ионы и полярные молекулы, на процессы гетеро-лиза и координации. Если в понятие молекулярности включить подобные электростатически участвующие молекулы, то в этом случае почти все реакции в растворах должны были бы описываться как полимолекулярные; подобная попытка была бы неудачной и привела бы к значительным затруднениям в выработке классификации. Поэтому при определении молекулярности учитываются только те молекулы, в которых происходит изменение ковалентности связей, а электростатические процессы с участием других молекул часто объединяются понятием сольватация. [40]
S N 1 или к Е2 - S N 2, но в пределах одного и того же кинетического порядка реакции соотношение продуктов реакции не зависит от концентрации реагента. [41]
Применяя реагирующие вещества в низких, примерно эквивалентных концентрациях в инертном растворителе ( бензоле), Свэну удалось определить кинетический порядок реакций трифенилгалоидметанов с различными нуклеофильными реагентами. [42]
Помимо того, что с помощью этого метода можно очень быстро проводить анализ продуктов, он позволяет также легко определять кинетический порядок реакции, энергии активации и теплоты адсорбции. Эффективность газовой хроматографии как метода установления природы и концентрации продуктов в различных реакциях уже доказана на примере большой серии катализаторов. [43]
Таким образом, из экспериментальных данных со всей очевидностью следует, что при разных температурах и соотношениях компонентов в ЦСК кинетический порядок реакции может быть также различным. Становится ясным поэтому, что для строгих сопоставлений активности ЦСК с различным фазовым составом необходимо изучение кинетических зависимостей протекания реакции. [44]
Ряд проведенных исследований по нитрованию ароматических соединений в различных органических растворителях мало продвинул вопрос о механизме реакции нитрования, так как не был установлен даже кинетический порядок реакции. Бенфолд и Инголд [2] нашли, что при применении большого избытка азотной кислоты с нитрометаном в качестве растворителя такие реакционноспособные соединения, как бензол, толуол и этилбензол, нитровались с одинаковой скоростью согласно закону для реакций нулевого порядка. [45]
Страницы: 1 2 3 4