Кинетический порядок - реакция
Cтраница 2
Как показали измерения, кинетический порядок реакции гидрирования бензола в присутствии MoS2 близок к нулевому по углеводороду и соответствует первому в отношении водорода. Температурный коэффициент скорости гидрирования бензола, измеренный в интервале 410 - 430, оказался равным 1 22, кажущаяся энергия активации Es 19250 кал / моль; для толуола, соответственно, - 1 29 и 24500 кал / моль. [16]
На практике широко пользуются понятием кинетический порядок реакции. Иногда имеется корреляция между молекулярностью и порядком реакции. [17]
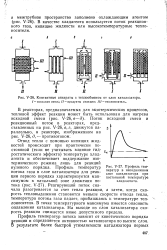 |
Контактные аппараты с теплообменом от слоя катализатора. / - исходная смесь. / / - продукты реакции. / / / - теплоноситель. [18] |
Профиль температур потока зависит от кинетического порядка реакции и определяется активностью катализатора по высоте слоя. [19]
Этим объясняется, вероятно, и нулевой кинетический порядок реакции. [20]
Вычислению скорости процесса должно предшествовать определение кинетического порядка реакции. [21]
Итак, в зависимости от способа обрыва кинетический порядок реакции может значительно изменяться и ингибирование НХ может становиться все более незначительным, в то время как обрыв, включающий R, приобретает все большее значение. На практике трудно отличить эти случаи один от другого, так как для этого величины концентрации Х2 должны быть очень невелики. [22]
Кенсмана, Ламара и Деминга с молибденом кинетический порядок реакции определялся нанесением на график обратной величины скорости реакции по величине PHj / PNHj, причем последнее отношение изменялось во время опыта от величины, соответствующей 15 % - ному распаду аммиака, до соответствующей 60 % - ному распаду. Результаты показывают определенное тормозящее действие продуктов реакции, но не дают возможности отличить тормозящее действие водорода от такого же действия азота. [23]
Поскольку стехиометрические коэфпцненты далеко не всегда определяют кинетический порядок реакции, при вычислениях скоростей химических превращений эти коэфициенты приходится заменять другими, находимыми опытом п называемыми кинетическими. [24]
Итак, в зависимости от способа обрыва кинетический порядок реакции может значительно изменяться и ингибирование НХ может становиться все более незначительным, в то время как обрыв, включающий R, приобретает все большее значение. На практике трудно отличить эти случаи один от другого, так как для этого величины концентрации Х2 должны быть очень невелики. [25]
На первый взгляд может показаться, что кинетический порядок реакции можно определить из стехиометрических коэффициентов реакции. [26]
При анализе вопроса о распределении зарядов необходимо различать кинетический порядок реакции и ее молекуляриость. Кинетический порядок касается лишь того порядка концентрации, котором должна быть пропорциональна наблюдаемая скорость реакции. Молекулярность реакции обозначает число молекул, принимающих участие в той или иной стадии реакции. Термин принимать участие интерпретируется по-разному, особенно с точки зрения участия растворителя. Другие авторы, например Свей [27], подчеркивают значение взаимодействий какого-либо реагента с растворителем или с другими растворенными веществами, вследствие чего он становится готовым к реакции. Взаимодействие со смежной молекулой, которую обычно считают инертной, способно, по всей вероятности, вызнать такое перераспределение заряда в молекуле перекиси водорода, что один конец молекулы становится положительнее другого; это облегчает возможность приближения другой молекулы или нона и его сольватацион-пой оболочки, а следовательно, и реакцию. [27]
Достоверно установленный факт, что в переходной области кинетический порядок реакции по кислоте возрастает с увеличением кислотности, со всей очевидностью вытекает из уравнения Блекэддера - Хиншельвуда, на основе которого фактически и проводилась количественная обработка всех кинетических результатов, полученных для переходной области. Эти результаты не согласуются с уравнением Дьюара, выведенным из его-теории л-комплекса, согласно которому порядок реакции по кислоте должен уменьшаться с увеличением кислотности. Более того, я-комплекс с нафталиновым остатком должен быть более устойчивым, чем с бензольным остатком, и при действии протона должен превращаться в конечные продукты труднее. Кинетический порядок по кислоте при переходе от гидразобензола к гидразо-нафталину не должен уменьшаться, а скорее должен был бы возрасти. Теория, клеточной диссоциации также не может объяснить эти данные, поскольку при таком механизме необходимо участие второго протона для создания электрической симметрии и ослабления связи N - N, что требуется для осуществления гомолиза. [28]
Выбор между этими механизмами нельзя сделать на основании кинетического порядка реакции, так как оба они отвечают реакции второго порядка. Однако эти два крайних случая в механизме реакции приводят к различным предсказаниям относительно стереохимии процесса. [29]
Выбор между этими механизмами нельзя сделать на основании кинетического порядка реакции, так как оба они отвечают реакции второго порядка. Однако эти два крайних случая н механизме реакции приводят к различным предсказаниям относительно стереохимии процесса. [30]
Страницы: 1 2 3 4