Бьеррум
Cтраница 1
Бьеррум и Поулсен [39] изучали неизмеримо быстрые реакции с помощью простой, но ранее не использованной методики охлаждения метанольных растворов реагентов примерно до - 100 и колориметрического наблюдения за ходом реакции. Цветные реакции, вроде реакции Ni ( II) с пиридином и Со ( II) или Fe ( lII) с ионом тиоцианата, имеют нормальные энергии активации ( 13 - 17 ккал), но необычно большие значения А5 ( от - 5 до 20 энгр. Проточная методика [35] показала, что AiS для реакции Fe3f - SC № составляет - 5 энтр. [1]
Бьеррум пытался установить, как переносилась метальная группа метионина в кислород лигнина: полностью ли ( как единица), или же сперва окислялась ( возможно - до формальдегида), а затем уже восстанавливалась. [2]
Бьеррум разработал метод, при использовании которого вначале рассчитывают ряд предварительных констант образования. [3]
Бьеррум полагает, что скорость реакции определяется термически индуцированным спонтанным мономолекулярным распадом комплекса, возникающего в результате столкновения между реагентами. Этот штосс-комплекс не является химическим соединением, а имеет чисто физическую природу. [4]
Бьеррум предположил, что d равно такому расстоянию, при котором вероятность нахождения ионов / в сферической оболочке толщиной dr минимальна ( [18], стр. [5]
Бьеррум [24] признавал, что теория полной ионизации должна быть модифицирована, чтобы она могла учитывать ионные пары. [6]
Бьеррум [19] рассматривал С как комплекс, получившийся при соударении частиц. [7]
Бьеррум в своей оригинальной работе [1] измерив коэффициент распределения ионов между водой и этанолом, считая при этом, что диффузионным потенциалом можно пренебречь. Почти 30 лет спустя он опубликовал теоретическую работу [6], в которой отмечал, что, поскольку нельзя определить контактную разность потенциалов, невозможно также точно определить коэффициенты распределения отдельных ионов. [8]
Бьеррум, развивая учение Льюиса, ввел коэффициент активности; он представляет собой величину, на которую надо умножить концентрацию, чтобы получить активность, или на которую надо умножить давление, чтобы получить летучесть. [9]
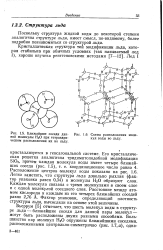 |
Ближайшие соседи данной молекулы Н2О при тетраэдри-ческом расположении их во льду.| Схема расположения молекул воды во льду. [10] |
Бьеррум [5] отмечает, что шесть молекул воды в структуре льда - ближайшие соседи для данной пары молекул - могут быть расположены двумя разными способами. [11]
Бьеррум первый обнаружил корреляцию между сродством ряда близкородственных лигандов к ионам водорода и их сродством к данному иону металла. [12]
Бьеррум предложил представлять константы ионизации аминокислот в цвиттерионной форме, когда константы ионизации кислот даны для групп NH, а константы ионизации основания - для групп СОО - - цвиттериона. [13]
Бьеррум принимает простейшую модель ионных растворов - он рассматривает ионы как несжимаемые и неполяризующиеся сферические частицы с радиусом а, находящиеся в среде с определенной макроскопической диэлектрической постоянной. При этом совершенно не учитываются неполярные квантовые связи между ионами, а также взаимодействие ионов с молекулами растворителя. [14]
Бьеррум [64] рассматривает процесс как статистический. [15]
Страницы: 1 2 3 4