Бьеррум
Cтраница 3
Бьеррум Я -, Образование амминов металлов в водном растворе. [31]
 |
Зависимость H ( r - f ( r. [32] |
Бьеррум предположил, что все ионы, оказавшиеся на расстоянии гг0 друг от друга, ассоциируют попарно, образуя ионные пары. [33]
Бьеррум ( 1926) указали, что при расчетах в теории Дебая - Гюккеля не учитывается возможность приближения противоположно заряженных ионов на такие расстояния, на которых энергия электростатического притяжения ионов оказывается больше энергии их теплового движения. В результате этого фактически образуется новая частица - ионная пара. Для растворов симметричных электролитов ионная пара в целом незаряжена, но обладает дипольным моментом. В растворах несимметричных электролитов ионные пары несут заряд, отличный от заряда ионов раствора, и возможна дальнейшая ассоциация с участием этих ионных пар. [34]
Бьеррум ( 1926) указали, что при расчетах в теории Дебая - Гюккеля не учитывается возможность приближения противоположно заряженных ионов на такие расстояния, на которых энергия электростатического притяжения ионов оказывается больше энергии их теплового движения. В результате этого фактически образуется новая частица - ионнаяпара. Для растворов симметричных электролитов ионная пара в целом не заряжена, но обладает дипольным моментом. В растворах несимметричных электролитов ионные пары несут заряд, отличный от заряда ионов раствора, и возможна дальнейшая ассоциация с участием этих ионных пар. [35]
Бьеррум предположил, что ионные пары образуются, если ионы сближаются на расстояние г / тш. Интегрирование функции Wdr в пределах от г, равного сумме радиусов ионов, до гт п позволяет найти долю ионных пар в растворе, а следовательно, и константу ассоциации Касс. Теория Бьеррума указывает, что вероятность образования ионных пар растет с ростом зарядов ионов и с уменьшением диэлектрической проницаемости растворителя. Подтверждение этих выводов было получено при изучении растворов феррицианида лантана LaFe ( CN) 6 в воде и в смесях воды с этанолом, гликолем, ацетоном, диоксаном и глицином, а также для растворов азотнокислого тетраизоамиламмония в различных смесях воды с диоксаном. [36]
Бьеррум [20] считал, что заряды амфиона достаточно пространственно разделены и поэтому он проявляет свойства двойных ионов. [37]
Бьеррум показал, что сольватационное равновесие в растворе [ Co ( NH3) e ] Cl3 устанавливается только в присутствии катализаторов. [38]
Бьеррум [77] рассматривает ионы типа /, находящиеся на расстояниях, меньших, чем а0, от центрального иона типа г, как ассоциированные, а ионы типа /, удаленные на расстояния, большие, чем а0 - как свободные и подчиняющиеся распределению Мильнера - Дебая. [39]
Бьеррум принимает простейшую модель ионных растворов - он рассматривает ионы как несжимаемые и неполяризующиося сферические частицы с радиусом а, находящиеся в среде с определенной макроскопической диэлектрической постоянной. При этом совершенно не учитываются неполярные квантовые связи между ионами, а также взаимодействие ионов с молекулами растворителя. [40]
Бьеррум в работе о константах диссоциации кислот учитывает взаимное влияние различных кислотных групп в многоосновных кислотах при помощи множителя Оствальда. [41]
Бьеррум обозначает через р обратную величину. [42]
Бьеррум, эффектом, определяемым уравнением ( 18), вставляя вместо ря я 1 только кулоновскую работу. Таким образом, получается, что электростатический эффект в системах с незаряженными ли-гандами всегда равен нулю по определению. [43]
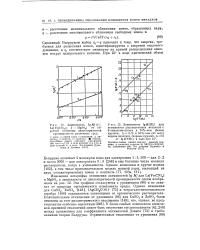 |
Зависимость IgJT ( ML для комплексов двухвалентных металлов с 8-окисихинолино. и в 70 % - ном ( белые кружки, Д 6 0 и 50 % - ном ( по весу водном диоксане ( черные кружки, Д 0. [44] |
Бьеррума включает 4 молекулы воды для электролита 1: 1, 500 - для 2: 2 и около 5000 - для электролита 3: 3 [248] и еще большие числа молекул растворителя, когда е уменьшается. [45]
Страницы: 1 2 3 4