Потенциал - ионизация - радикал
Cтраница 1
Потенциалы ионизации радикалов могут быть также определены косвенным путем. Из выражения для потенциала появления осколочного иона ( 10) следует, что потенциал ионизации радикала / ( R может быть вычислен, если известны потенциалы появления осколочного иона AP ( Rf), энергия связи D ( Ri - R2) и Екш осколков. [1]
Потенциалы ионизации радикалов в тех случаях, когда последние в виде отдельных частиц впускаются в ионизационную камеру, определяются теми же методами, что и потенциалы ионизации молекул. Обычно радикалы получаются при пиролизе галоидозамещенных молекул, легко теряющих атом галоида. Пиролиз производится в непосредственной близости от области ионизации, так что радикалы попадают в нее практически без столкновений. [2]
Потенциалы ионизации диалкилазотокисных радикалов ( вертикальные, 7 24 - 7 4 эВ [ 7а б ], адиабатические, 6 7 - Ь 6 8 эВ [76]) меньше, чему соответствующих аминов и гидроксиламинов. [3]
Предел ридберговских серий дает потенциал ионизации радикала, но не обязательно самый низкий потенциал ионизации. [4]
В других случаях при измерении потенциалов ионизации радикалов их получают внутри ионизационной камеры. Например, Уолдрон [2105] описывает источник, который содержит, наряду с вольфрамовой нитью для образования бомбардирующих электронов, платиновую проволоку, помещенную на пути вводимого образца. [5]
 |
Потенциалы ионизации замещенных бензолов. [6] |
Это может быть вызвано увеличением потенциала ионизации замещенного фениль-ного радикала, возрастанием прочности связи С-F либо, наконец, повышением кинетической энергии или энергии возбуждения. [7]
В этом случае определение потенциала появления дает потенциал ионизации радикала R2 или энергию диссоциации Z ( Ri - R2) при условии, что одна из этих величин уже известна. Если же неизвестны обе эти величины, то путем комбинирования тщательно подобранных потенциалов появления можно исключить одну из них и получить интересующую нас термохимическую величину. [8]
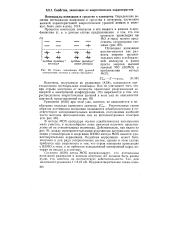 |
Схема заполнения МО уровней приближении метода. [9] |
Согласно (8.58) метод МОХ предсказывает, что потенциалы ионизации радикалов и анионов нечетных АУ должны быть равны нулю, что, конечно, не соответствует действительности. [10]
D - прочность связи С - Н, / с - потенциал ионизации радикала, образующегося при присоединении водорода к виниловому соединению. [11]
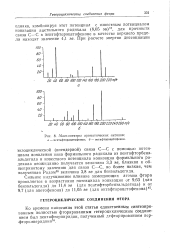 |
Масс-спектры ароматических кетонов. [12] |
С-С с помощью потенциала появления иона формильного радикала из пентафторбенз-альдегида и известного потенциала ионизации формильного радикала неожиданно получается величина 3 3 эв, близкая к общепринятому значению для связи С-С, но более низкая, чем полученная Ридом58 величина 3 8 эв для бензальдегида. [13]
Следовательно, для измерения энергии разрыва связи нужно решить экспериментально очень сложную задачу - найти потенциал ионизации радикала. Обычный - способ заключается и том, чтобы создать радикалы пиролизом или фотолизом нестойкой молекулы и при этом сделать возможно более коротким расстояние между источником радикалов и ионизирующим электронным пучком. Необходимо, чтобы при переносе радикалов из области высокого давления, в которой они зарождаются, в область низкого давления ионного источника масс-спектрометра не успевали протекать побочные реакции. Для разделения этих областей обычно применяют мембрану с малым отверстием, но рекомбинация радикалов на поверхности мембраны может иногда препятствовать изучению очень реакционно-способных и нестойких радикалов, как, например, метиленового. [14]
Тем не менее Дайблер38 полагает, что можно приблизительно вычислить энергию связи С-F, если принять значение потенциала ионизации пентафторфенильного радикала равным 10 6 эв. Эту величину находят в предположении, что разность потенциалов ионизации пентафторфенила и гексафторбензола равна разности потенциалов ионизации фенила и бензола. Потенциал ионизации бензола составляет 9 2 эв, для фенильного радикала Кандел46 нашел значение 9 9 эв. [15]
Страницы: 1 2 3