Потенциал - ионизация - радикал
Cтраница 2
Мы изучаем потенциалы ионизации замещенных бензильных свободных радикалов, и, хотя эта работа еще не закончена, нами было найдено, что между потенциалом ионизации радикала и константой 0 существует весьма хорошая линейная зависимость. [16]
До последнего времени наиболее распространенным методом качественного обнаружения свободных радикалов является метод ионизации электронами с низкой энергией, недостаточной для диссоциативной ионизации молекул, но большей, чем потенциал ионизации радикалов. Этот метод был впервые применен Эльтен-тоном [6] именно для анализа свободных радикалов. Однако при таких энергиях сечения ионизации малы, а практически достигаемые токи электронов составляют 1 - 10 % от токов, применяемых в ионных источниках при обычных методах ионизации. [17]
Развитие исследований фотоионизационных процессов с помощью комбинации вакуумного монохроматора с масс-спектрометром [13, 14] дает возможность с большой точностью определять энергию диссоциации связей в молекулах и образующихся ионах, теплоты образования ионов и радикалов и потенциалы ионизации радикалов. [18]
СХ) - частота колебания; Я ( СХ) - равновесное межядерное расстояние в СН3Х ( см. табл. 17); К ( СН3Х) - теплота диссоциации СН3Х на СН3 и X ( см. табл. 17); Л ( ион) Л ( С) Я ( Х -) 0 56 Я ( Х -) [7,118]; ЭС ( X) - электронное сродство атома X [83]; I ( СН3) - потенциал ионизации радикала метила180 ккал. [19]
Если мы примем, что потенциал ионизации радикала неопентила близок к потенциалу ионизации н-пропи-ла, определенному Лоссингом [9] и равному 8 69 в, то мы сможем оценить A. Эта оценка дает величину около 205 ккал / молъ. Так как реакция идет очень быстро, она, конечно, не может быть эндотер-мичной, и, следовательно, ион амила должен перестраиваться в реакции. [20]
Таким образом, измерив кинетическую энергию иона Ri ( например, по методу задерживающего потенциала), по формуле ( 14) получают Ей по формуле ( 12) - искомую энергию связи D. Входящий в формулу ( 12) потенциал ионизации радикала Ri может быть измерен непосредственно методом электронного удара, что впервые было осуществлено Дж. [21]
Все более широкое применение для исследования свободных радикалов находит масс-спектрометрия, позволяющая из анализа масс-спектров ионов определять природу радикалов и их концентрации. Применение ее основано на том, что потенциал ионизации радикалов понижен по сравнению с потенциалом ионизации молекул на величину порядка энергии связи радикала в молекуле. [22]
На основании этих данных мы смогли вычислить величину потенциала ионизации третга-бутильного радикала, которая оказалась равной около 7 4эв, что очень хорошо согласуется с прямыми измерениями, проведенными в данной работе. [23]
Возможность обнаружения свободных радикалов основана на том, что потенциалы ионизации радикалов меньше потенциала появления лона пз молекулы на величину энергии связи. Для того чтобы радикалы попадали в область ионизации без соударений, применяется техника молекулярных пучков. Непрерывный анализ реагирующей газовой смеси позволяет следить за ходом реакции. Если скорость реакций велика, применяют импульсные масс-спектро-скопы ( с осциллографич. [24]
Потенциалы ионизации радикалов могут быть также определены косвенным путем. Из выражения для потенциала появления осколочного иона ( 10) следует, что потенциал ионизации радикала / ( R может быть вычислен, если известны потенциалы появления осколочного иона AP ( Rf), энергия связи D ( Ri - R2) и Екш осколков. [25]
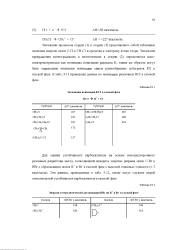 |
Энтальпии ионизации RC1 в газовой фазе. [26] |
Энтальпии процессов стадии ( 1) и стадии ( 3) представляют собой табличные значения энергии связи С - С1 в СН3С1 и сродства к электрону атома хлора. Энтальпия превращения метил-радикала в метил-катион в стадии ( 2) определяется масс-спектрометрически как потенциал ионизации радикала R, таким же образом могут быть определены энтальпии ионизации самых разнообразных субстратов RX в газовой фазе. В табл. 9.11 прнаедены данные по ионизации различных RC1 в газовой фазе. [27]
Энтальпии процессов стадии ( 1) и стадии ( 3) представляют собой табличные значения энергии связи С - С1 в СН3С1 и сродства к электрону атома хлора. Энтальпия превращения метил-радикала в метил-катион в стадии ( 2) определяется масс-спект-рометрически как потенциал ионизации радикала R, таким же образом могут быть определены энтальпии ионизации самых разнообразных субстратов RX в газовой фазе. В табл. 9.11 приведены данные по ионизации различных RC1 в газовой фазе. [28]
В 1955 г. Фонер и Гадсон [87] экспериментально определили QH-но Для получения больших количеств Н02, анализируемых масс-спектрометром, была использована реакция Н2О2 с радикалами, получающимися в разряде в парах воды. Энергия диссоциации Н - Н02 была определена как разность между потенциалом появления HOJ и потенциалом ионизации радикала НО2 и оказалась равной 89 5 ккал. При помощи этой величины и термохимических данных была рассчитана QH O равная 47 1 ккал. НО 91 ккал и QJJ-о 45 ккал неплохо совпадают с экспериментальными значениями. [29]
Поведение п-метоксито-луола при взаимодействии с электронами несколько отличается от выше рассмотренных соединений. Это объясняется, очевидно, высокой стабильностью л-метокситолил-катиона, а также тем, что под влиянием сильно донорной групп ОСНз потенциал ионизации радикала НзСО - - РН-СН2 значительно уменьшается. Его малая интенсивность обусловлена, по-видимому, крайней нестабильностью М 2, вследствие чего он подвергается быстрому распаду. [30]
Страницы: 1 2 3