Потенциал - ионизация - радикал
Cтраница 3
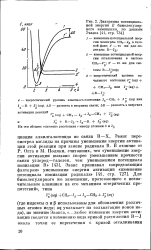 |
Диаграмма потенциальной энергии Е бимолекулярного замещения, по данным Эванса [ 41, стр. 734 ]. [31] |
Поляни, считавших, что уменьшение энергии активации вызвано скорее уменьшением прочности связи углерод - галоген, чем уменьшением потенциала ионизации R [43], Эванс признавал определяющим фактором уменьшения энергии активации изменение потенциала ионизации радикала [ 41, стр. [32]
 |
Потенциалы ионизации некоторых простейших молекул и радикалов. [33] |
Для процессов типа ( 3.1, а) следует сравнивать потенциалы ионизации двух радикалов, а в случае ( 3.1 6) - двух молекул. Правило это имеет сугубо качественный характер и применимо только к простейшим органическим молекулам, когда известна диссоциирующая связь. Использование данного правила также ограничивается отсутствием достаточно подробных сведений о потенциалах ионизации радикалов разного состава и структуры. Кроме того, дальнейший распад первичных осколочных ионов может существенно искажать ожидаемое соотношение интенсивностей их пиков. [34]
Как видно из таблицы, в масс-спектрах соединений первой и второй групп соотношение интенсивностей пика арилметиленового катиона к молекулярному ( [ М - Н ] ДМ ]) уменьшается с понижением ионизирующего напряжения. Поведение п-метоксито-луола при взаимодействии с электронами несколько отличается от выше рассмотренных соединений. Это объясняется, очевидно, высокой стабильностью / г-метокситолил-катиона, а также тем, что под влиянием сильно донорной групп ОСН3 потенциал ионизации радикала НзСО - - РН-СН2 значительно уменьшается. Его малая интенсивность обусловлена, по-видимому, крайней нестабильностью М 2, вследствие чего он подвергается быстрому распаду. [35]
 |
Относительные активности радикалов LR плотности неспаренного электрона на реакционном центре р и уровни орбитали неспаренного электрона е, рассчитанные по методу CNDO / SP. [36] |
Кроме того, естественно ожидать, что реакционная способность радикала, даже в простом рассмотрении, должна зависеть е только от сп, но и от уровня МО неспаренлого электрона. Это легко пояснить на примере двух рассмотренных выше простейших радикальных реакций. Действительно, вторая стадия в каждой из них, связанная с делокализацией иеспаренного электрона в атакуемую систему, будет проходить тем легче, чем меньше потенциал ионизации радикала. [37]
Удивительно, что найденные потенциалы ионизации столь низки. Действительно, это, вероятно, самые низкие значения из известных до сих пор потенциалов ионизации свободных радикалов. Это дает возможность предположить, что в процессах, на основании которых определяли теплоты образования свободных радикалов, возможно, выделяется некоторая избыточная энергия, а пренебрежение ею приводит к тому, что вычисленные значения потенциалов ионизации радикалов оказываются заниженными. Однако наличие неучтенной энергии вряд ли даст ошибку, превышающую 1 эв, но даже при ошибке такого порядка получающиеся значения теплот образования приводят к очень низким значениям потенциалов ионизации. К сожалению, потенциалы ионизации радикалов CH3NH и ( CH3) 2N довольно трудно вычислить. В наших расчетах теплот образования этих радикалов было использовано найденное Колленом [9] значение AHf [ ( CH3) 2N ] 227 ккал / молъ. Он же дает для величины AHf ( CH3N H) значение 226 ккал / молъ. [38]
Удивительно, что найденные потенциалы ионизации столь низки. Действительно, это, вероятно, самые низкие значения из известных до сих пор потенциалов ионизации свободных радикалов. Это дает возможность предположить, что в процессах, на основании которых определяли теплоты образования свободных радикалов, возможно, выделяется некоторая избыточная энергия, а пренебрежение ею приводит к тому, что вычисленные значения потенциалов ионизации радикалов оказываются заниженными. Однако наличие неучтенной энергии вряд ли даст ошибку, превышающую 1 эв, но даже при ошибке такого порядка получающиеся значения теплот образования приводят к очень низким значениям потенциалов ионизации. К сожалению, потенциалы ионизации радикалов CH3NH и ( CH3) 2N довольно трудно вычислить. В наших расчетах теплот образования этих радикалов было использовано найденное Колленом [9] значение AHf [ ( CH3) 2N ] 227 ккал / молъ. Он же дает для величины AHf ( CH3N H) значение 226 ккал / молъ. [39]
Замечание, добавленное при корректуре. На основании этого значения и значения ( N2HJ) из гидразина, полученного нами, вычислено значение энергии связи N - Н, равное примерно 76 ккал / молъ, которое вполне приемлемо. Поскольку это также привело к более низкому значению теплоты образования гидразильного радикала, чем полученное в результате наших косвенных измерений, мы были вынуждены заключить, что в значение A ( CR), которое мы получили, входит некоторое количество избыточной энергии. Поэтому значения энергий связей, приведенные в табл. 8, потенциалы ионизации радикалов, приведенные в табл. 10, и относящиеся к ним рассмотрения должны быть в соответствующей степени изменены. [40]
Он пришел к выводу, что первичной электродной реакцией является разряд карбоксилата с одновременным отщеплением двуокиси углерода и образованием алкильного радикала. Если этот радикал легко окисляется при наложенном потенциале, то будет иметь место механизм, включающий образование карбониевого иона. Если радикал окисляется медленно, то может образовываться димер Кольбе. Эберсон предположил, что результат можно предсказать, если известен потенциал ионизации радикала; при потенциале более 8эВ осуществляется радикальный механизм, при потенциале меньше 8эВ - механизм с участием карбо иевого иона. [41]
Если в результате реакции получаются только стабильные молекулы, то используются обычные методы анализа. Однако очень часто на раскаленных проволоках образуются свободные радикалы. В таких случаях количественные измерения возможны только для наиболее тяжелых радикалов, поскольку для образующихся одновременно более легких радикалов неизвестен вклад в их масс-спектр тяжелых радикалов. Так, например, пропан на раскаленной платине дает пропильный радикал, обнаруживаемый по увеличению пика ионов С3Н, , образующихся при ионизации радикалов. Радикалы С2Н5 и СН3 могли бы быть определены при измерениях ионного тока в опытах, в которых энергия электронов была бы ниже потенциала появления осколочных ионов, но превосходила потенциалы ионизации радикалов. Потенциал же появления осколочного иона из более тяжелого радикала может быть ниже, чем потенциал появления этого иона из молекулы. Следовательно, метод ионизации электронами низкой энергии дает только качественные результаты. Для количественных измерений необходимо знать масс-спектры различных радикалов. Масс-спектр свободного радикала может быть получен, если будет найдена реакция, в которой образуется только один указанный радикал, и при этом не будут идти ни параллельные, ни вторичные реакции. Такая простая картина обычно не наблюдается, и всегда возникают различные осложнения. Образованные первичные продукты могут реагировать на горячей каталитической проволоке. Радикалы могут вступать в реакцию на электродах в ионном источнике. Эти эффекты уменьшаются, когда величина KLalS мала. Вероятно, они могут быть исключены при использовании методики молекулярного пучка. Еще одна трудность, возникающая при исследовании реакций углеводородов на металлических проволоках, заключается в том, что одновременно с образованием радикалов может идти полное разложение этих соединений до углерода ( или карбида) и водорода. Тогда невозможно свести полный материальный баланс, основанный на предположении, что каждая молекула углеводорода дает при реакции один радикал. [42]
Страницы: 1 2 3