Потенциал - катализатор
Cтраница 1
Потенциал катализатора смещается в анодную сторону всегда на 120 - 140 мв и, следовательно, значительная доля поверхности покрыта водородом. Скорость реакции лимитируется при малой концентрации щелочи активацией непредельного соединения, и энергия ( активации составляет 2 - 3 ккал / моль. При больших концентрациях щелочи воспроизводство водорода, принимающего участие в реакции, настолько замедляется, что реакция лимитируется уже атомиза-цией водорода и энергия активации доходит до 13 ккал / моль. Скорость реакции особенно мала, потому что большая часть поверхности занята прочно связанным водородом, а а реакционноспособной части поверхности водород атомизируется с малой скоростью. [1]
Потенциал катализатора при внесении карбинола сразу смещается на) 1в, но затем падает и достигает стационарного состояния 0 020в по обратимому водородному электроду в данном растворе. [2]
 |
Влияние степени удаления водорода фенилацетиленом на сопротивление Pt - и Pd-черней и. [3] |
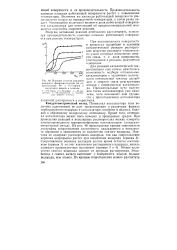
Потенциал катализатора ( как величина аддитивная) не дает представления о различных формах сорбированного водорода в катализаторе, особенно в области, близкой к обратимому водородному потенциалу. Кроме того, потенциал катализатора может быть измерен в проводящих средах. На рис. 48 представлены кривые зависимости логарифма сопротивления платинового, палладиевого и никелевого порошков в зависимости от количества снятого водорода. Общее количество снятого водорода зависит от природы растворителя. Этил-бензол с самого начала вытесняет с поверхности никеля больше водорода, чем этанол. [4]
Падение потенциала катализатора в анодную сторону и скорость поглощения водорода из газовой фазы зависит от природы заместителей в ядре и их положения. [5]
Измерения потенциала катализатора при гидрировании бензола в растворах показало, что бензол слабо адсорбируется и. Поэтому применение любых, хорошо адсорбирующихся растворителей должно замедлить реакцию. Обычно катализаторы, например платиновые, после приготовления недостаточно тщательно отмываются от посторонних ионов, в частности щелочных. Так, например, в присутствии 0 2 г окиси платины скорость гидрирования 15 мл бензола при 45 С составляла 8 - 11 мл / мин, а 0 2 мл бензола в 15 мл уксусной кислоты - только 2 5 мл / мин. [6]
Измерение потенциала катализатора позволяет точно определить критические точки реакции гидрирования смеси непредельных соединений. Из рис. 6, например, видно, что кинетическая кривая восстановления гек-сина-1 на Ni не имеет экстремальных точек и перегибов и не отражает сложных изменений в составе катализата и структуре катализатора; напротив, четкий минимум на потенциальной кривой совпадает с исчезновением из раствора ацетиленового углеводорода. [7]
 |
Гидрирование гексена-1 в буферном растворе на Pt-черни. [8] |
Измерение потенциала катализатора в ходе гидрирования позволяет судить о соотношении концентраций реагирующих веществ на поверхности катализатора [7] и приближенно оценить степень заполнения ее водородом [11], а следовательно, и энергию связи водорода, принимающего участие в реакции. [9]
Измерение потенциала катализатора позволяет точно определить критические точки реакции гидрирования смеси непредельных соединений. Из рис. 6, например, видно, что кинетическая кривая восстановления гек-сина-1 на Ni не имеет экстремальных точек и перегибов и не отражает сложных изменений в составе катализата и структуре катализатора; напротив, четкий минимум на потенциальной кривой совпадает с исчезновением из раствора ацетиленового углеводорода. [10]
Измерение потенциала катализаторов гидрогенизации оказалось возможным вследствие того, что на поверхности переходных металлов с расстояниями между узлами кристаллической решетки 3 3 - 3 6 А молекулы водорода растягиваются на атомные пары и отдельные атомы. Благодаря стремлению адсорбированного водорода перейти в раствор возникает разность потенциалов, зависящая от концентрации ионов водорода в растворе, давления и температуры. [11]
Измерение потенциала катализаторов гидрогенизации оказалось возможным вследствие того, что на поверхности переходных металлов с расстояниями между узлами кристаллической решетки 3 3 - 3 6 А молекулы водорода растягиваются на атомные пары и отдельные атомы. Благодаря стремлению адсорбированного водорода перейти в раствор возникает разность потенциалов, зависящая от концентрации ионов водорода в растворе, давления и температуры. [12]
 |
Прибор для потенциометри. [13] |
Между смещением потенциала катализатора и степенью заполнения поверхности водородом ( в пределах водородной-области кривой заряжения) наблюдается линейная зависимость, что отвечает логарифмической изотерме адсорбции. В соответствии с этим была установлена линейная зависимость энергии активации реакций гидрирования от смещения потенциала. [14]
В процессе реакции потенциал катализатора остается близким к обратимому водородному в данном растворе. Гидрирование протекает при почти полном покрытии поверхности катализатора водородом. Такой случай отвечает первому порядку реакции по-непредельному соединению и нулевому или дробному по водороду. Он реализуется для веществ, слабо вытесняющих водород с поверхности ( гексен, замещенные олефины и др.), уже при обычном давлении, особенно легко - в щелочных растворах. Для веществ, легко и быстро снимающих водород с поверхности катализатора ( ацетилен и его производные, нитросоединения, соединения с сопряженными связями), нулевой порядок по водороду, когда скорость его воспроизводства на поверхности больше скорости снятия, устанавливается при давлениях порядка 40 - 60 атпи. Энергия активации зависит от строения непредельных соединений и колеблется в пределах 4 - 9 ккал / молъ для ацетиленовых и этиленовых углеводородов соответственно. [15]
Страницы: 1 2 3 4 5