Потенциал - катализатор
Cтраница 4
Казалось бы, что при значительных катодных смещениях потенциалов катализатора лимитирующей стадией реакции должна быть активация кислорода и скорость реакции будет понижаться с увеличением концентрации спирта. [46]
 |
Схема установки восстановления МХНБ на платинированном угле. [47] |
На основании наблюдавшегося незначительного ускорения реакции и увеличения смещения потенциала катализатора при повышении концентрации нитробензола, а также отрицательного температурного коэффициента Шмонина сделала вывод, что процесс восстановления нитробензола на платиновой черни в растворе 50 % - ного этанола лимитируется активацией нитросоединения. [48]
Изучено окисление водных растворов этанола на платиновой черни с измерением потенциала катализатора. Показано, что кислород, предварительно адсорбированный на поверхности катализатора, является чрезвычайно реакци-ионноспособным, обусловливая инициирование процесса и поддержание его скорости на соответствующем уровне. Отмечено торможение процесса продуктом реакции-уксусной кислотой. Прямая пропорциональность между скоростью окисления и количеством катализатора исключает возможность цепного механизма. Это подтверждается отсутствием перекисных соединений в реакционной смеси и низким порядком реакции по обоим компонентам процесса. [49]
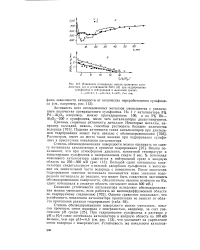 |
Изменение потенциала никель-хромового катализатора ( а и устойчивости NiCr ( б при гидрировании сульфолена в нейтральной и щелочной средах. У -. рН - 6 5. 2 - рН 10 4. Г-20 С. Р1 атм. [50] |
При гидрировании сульфолена в растворе с рН - 10 4 сдвиг потенциала катализатора в анодную область на 100мВ меньше, чем при рН 6 5 ( см. рис. 113), что указывает на укрепление-связи водорода с поверхностью. [51]
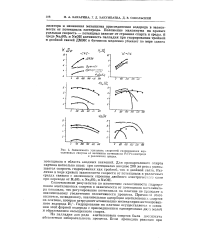 |
Зависимость удельных скоростей гидрирования ацетиленовых спиртов от величины потенциала Pd / Pt-электрода в различных средах. [52] |
Сопоставление результатов по изменению селективности гидрирования ацетиленовых спиртов в зависимости от потенциала катализатора показало, что регулирование потенциала на платине не приводит к значительному увеличению селективности процесса. Гидрирование на платине осуществляется з основном этой формой водорода с присоединением одновременно двух молей и образованием насыщенного спирта. [53]
Количество водорода, которое поглощено из газовой фазы к моменту резкого подъема потенциала катализатора вследствие насыщения его водородом тем больше, чем больше давление. [54]
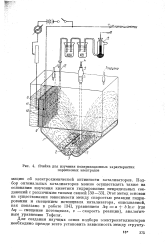 |
Ячейка для изучения поляризационных характеристик порошковых электродов. [55] |
Этот метод основан на существовании зависимости между скоростью реакции гидрирования и смещением потенциала катализатора, описываемой, как показано в работе [34], уравнением Афа Ыш; ( где Аф - смещение потенциала, v - скорость реакции), аналогичным уравнению Тафеля. [56]
Энергия ( активации может быть с известным приближением вычислена при знании падения потенциала катализатора ДЯ от обратимого - водородного в анодную сторону: Л А. [57]
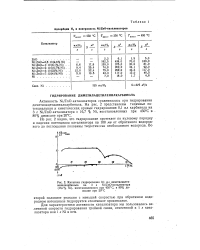 |
Кинетика гидрирования 0 1 мл диметилацетиленилкарбинола на 3 г Ni / ZnO-катализатора ( 16 7 % Ni, восстановленного при 450 С, в 80 % диоксане при 20 С i. [58] |
Из рис. 2 видно, что гидрирование протекает по нулевому порядку и падении потенциала катализатора на 100 мв от обратимого водородного до поглощения половины теоретически необходимого водорода. [59]
Электрохимический метод исследования кинетики жидкофазных каталитических реакций основан на том, что, измеряя потенциал катализатора и используя кривые заряжания для данного металла в данном растворителе, можно с достаточной точностью определить концентрацию сорбированного газа ( водорода, кислорода) на поверхности катализатора. [60]
Страницы: 1 2 3 4 5