Потенциал - медь
Cтраница 3
В результате образования комплекса концентрация ионов Си настолько снижается, что потенциал меди становится положительным по отношению к потенциалу водорода. [31]
Кроме того, такое различие не является следствием малой точности измерения потенциала меди в исследованном растворе. На неудовлетворительную воспроизводимость величины потенциала в разбавленных цианистых растворах, содержащих значительный избыток свободного цианида, указывал Шпитцер [210], который, однако, отметил, что при увеличении концентрации электролита эта воспроизводимость улучшается. [32]
При этом все примеси, имеющие электродный потенциал более положительный, чем потенциал меди ( величина ф в уравнении Нернста), выпадают в виде осадка ( шлама) на дно электролитической ванны. Среди примесей в меди нередко содержатся золото, серебро, платина, селен, теллур, представляющие большую ценность как драгоценные металлы и полупроводники. Таким образом, извлечение их из шлама в значительной степени компенсирует затраты электроэнергии на рафинирование меди. [33]
Для гальванической ванны, к которой относятся данные приведенные на рис. 6.4, потенциал меди составляет 0 042 В. Длительное нахождение деталей в гальванической ванне приводит лишь к слабому растворению меди, сопровождающемуся восстановлением растворенного кислорода в качестве катодной реакции. Это растворение не мешает получению удовлетворительного никеля покрытия и полностью подавляется в случае погружения деталей в ванну под током. Проблема нанесения подслоя меди решается путем использования комплексной медноцианистой ванны. [35]
Применяют комплексные, главным образом цианистые, соли этих металлов, в которых потенциал меди значительно смещается в сторону отрицательных значений, приближаясь к потенциалу выделения цинка. Как видно из рис. ХП-23, суммарная поляризационная кривая выделения сплава до плотности тока 1 2 А / дм2 располагается в менее отрицательной области по сравнению с кривыми раздельного восстановления ионов меди и цинка, что указывает на облегчение процесса, обусловленное сплавообразованием. [36]
Золото и серебро, а также металлы платиновой группы, потенциалы которых более положительны, чем потенциал меди, почти полностью выпадают в шлам. [37]
Если концентрация ионов этого металла к концу выделения меди составит 1 г-ион / л, то потенциал меди в этом растворе будет равен этой же величине, так как процесс осаждения ее прекратится, очевидно, тогда, когда электродные потенциалы этих металлов сравняются. [38]
Золото и серебро, а также металлы платиновой группы, потенциалы которых более положительны, чем потенциал меди, почти полностью выпадают в шлам. [39]
Контакт меди с нержавеющей сталью приводит к дальнейшему уменьшению потенциала коррозии нержавеющей стали по отношению к потенциалу меди из-за уменьшения катодной поляризации стали, поскольку сталь является катодом в биметаллической паре нержавеющая сталь - медь. Таким образом, контакт стали с медью приводит к протеканию МКК стали при постоянном потенциале, медь в данном случае действует аналогично потен-циостату. [40]
Вторая группа примесей - As, Sb, Bi являются наиболее вредными вследствие близости их потенциалов к потенциалу меди и влиянию на качество катодной меди. Ионы этих элементов, образующиеся при анодном растворении меди, накапливаются в растворе. [41]
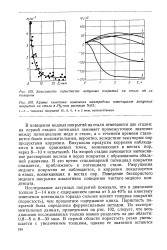 |
Зависимость пористости латунных покрытий на стали от их толщины.| Кривые кинетики изменения электродных потенциалов латунных покрытий на стали в 3 % - ном растворе NaCl. [42] |
В поведении медных покрытий на стали отмечаются две стадии: на первой стадии потенциал занимает промежуточное значение между потенциалами меди и стали, а с течением времени становится более положительным, вероятно, вследствие закупорки пор продуктами коррозии. Визуально продукты коррозии наблюдаются в виде оранжевых точек, возникающих в местах пор, через 8 - 10 ч испытаний. На второй стадии начинается интенсивное растворение железа в порах покрытия с образованием обильной ржавчины. В это время стационарный потенциал покрытия снижается, приближаясь к потенциалу стали. Разрушения медного покрытия не наблюдается, и коррозия локализуется в язвах, возникающих в местах пор. Поведение беспористого медного покрытия аналогично поведению чистого медного конденсата. [43]
Равикович показали, что при одновременном введении в раствор гуммиарабика и крезолсульфо-новой кислоты можно настолько изменить и сблизить между собой потенциалы меди, цинка и никеля, что становится возможным их совместное осаждение в виде сплава. [44]
Поскольку в данном случае изменением концентрации двухвалентной меди за счет образования одновалентной меди можно пренебречь, очевидно, что все отклонение потенциала меди от равновесного значения в первый период времени после добавки обусловлено пониженным значением концентрации Си в объеме раствора. [45]
Страницы: 1 2 3 4
