Потенциал - никель
Cтраница 2
 |
Зависимость состава сплава олово - никель от плотности тока. [16] |
При этом равновесный и катодные потенциалы олова приобретают более электроотрицательные значения, чем потенциалы никеля. Благодаря этому при определенных плотностях тока достигается сближение потенциалов выделения металлов на катоде. Совместному осаждению олова и никеля способствует также деполяризация при разряде ионов обоих металлов вследствие образования химического соединения NiSn и уменьшения парциальной молярной свободной энергии системы. Однако на свойства осадков ( особенно на внутренние напряжения в них) температура и рН раствора оказывают существенное влияние. [17]
Стандартные потенциалы олова и никеля различаются примерно на 0 1 В, причем потенциал никеля отрицательнее потенциала олова. Катодная поляризация при электролизе растворов солей ( сульфатов, хлоридов) выражена значительно резче для никеля, чем для олова. Если же к хлоридному электролиту добавить фторид натрия или аммония, то стационарные и катодные потенциалы выделения олова приобретают более отрицательные значения, чем потенциалы никеля в таком же растворе. [18]
 |
Цинковый электрод. [19] |
Величина и знак потенциала зависят от свойств металла, от его энергии кристаллической решетки; например, потенциал цинка значительно более отрицателен, чем потенциал никеля, кобальта, меди и других металлов, потенциалы которых определены при одних и тех же условиях. [20]
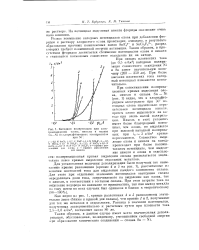 |
Катодная поляризация при элок. [21] |
При сопоставлении поляризационных кривых выделения олова, никеля и сплава Sn - Ni ( рис. 1) видно, что в хлоридфто-ридном электролите при 50 потенциал олова значительно отрицательнее потенциала никеля, причем олово выделяется на катоде при очень малой поляризации. Никель в этих условиях имеет более благородный потенциал, чем олово, но выделяется при высокой катодной поляризации; при г I, - 3 а / дмг кривые пересекаются. Совместное выделение олова и никеля на катоде происходит при более положительном потенциале, чем выделение никеля и олова в отдельности: поляризационная кривая выделения сплава располагается значительно левее кривых выделения отдельных металлов. [22]
В растворах простых солей только немногие металлы имеют близкие значения равновесных потенциалов. Например, потенциалы никеля и кобальта в сернокислых растворах, свинца и олова в борфтористоводородных растворах столь близки, что совместное осаждение их на катоде возможно при самых низких значениях плотности тока. В то же время равновесные потенциалы меди и цинка отличаются более чем на 1 В и при невысокой плотности тока на катоде будет выделяться только медь. [23]
Потенциал растворения твердого раствора никеля с его примесями при невысоком содержании последних будет сравнительно мало отличаться от потенциала растворения чистого никеля. Причем, если медь сдвигает потенциал никеля в электроположительную, то железо, наоборот, сдвигает этот потенциал в электроотрицательную сторону. Равновесные потенциалы сульфидов меди и никеля не устойчивы и не всегда воспроизводимы. [24]
Сульфат-ион препятствует также активации никеля хлорид-ионами. Однако при соотношении cNaCi: Ска2зо4 1: Ю никель находится еще на границе активно-пассивного состояния; потенциал никеля при анодной поляризации в этом растворе очень неустойчив и колеблется в широких пределах. [25]
Сульфат-ион препятствует также активации никеля хлорид-ионами. Однако при соотношении CNaci CNa Oi 1: 10 никель находится еще на границе активно-пассивного состояния; потенциал никеля при анодной поляризации в этом растворе очень неустойчив и колеблется в широких пределах. [26]
Потенциалы никелированных образцов ( рис. 47, б), как и медненых, располагаются между потенциалами подложки и покрытия. Однако, в отличие от меди, при увеличении толщины никелевого покрытия до 50 мкм не удается полностью исключить электрохимическое влияние основы и получить совпадение потенциала электрода и потенциала никеля. При малых толщинах никелевого покрытия ( 1, 5 и 10 мкм) потенциал разблагораживается, а при более толстых слоях облагораживается во времени, что указывает, соответственно на ускорение и замедление анодной реакции в порах. [27]
Потенциалы никелированных образцов ( рис. 47, б), как и медненых, располагаются между потенциалами подложки и покрытия. Однако, в отличие от меди, при увеличении толщины никелевого покрытия до 50 мкм не удается полностью исключить электрохимическое влияние основы и получить совпадение потенциала электрода и потенциала никеля. При малых толщинах никелевого покрытия ( 1 5 и 10 мкм) потенциал разблагораживается, а при более толстых слоях облагораживается во времени, что указывает, соответственно на ускорение и замедление анодной реакции в порах. [28]
Нормальный потенциал никеля примерно на 0 1 В электроотрицательнее потенциала олова, причем катодная поляризация при электроосаждении никеля выражена значительно резче, чем при электролизе сульфата или хлорида олова. Если к хлоридному электролиту добавить фториды натрия и аммония, то стационарный и катодный ( до некоторого значения / к) потенциалы олова приобретают более электроотрицательные значения, чем потенциалы никеля в таком же растворе. [29]
Многослойные в два-три слоя никелевые покрытия обладают большей коррозионной стойкостью, чем однослойные. Первый слой никеля осаждают из простого никелевого электролита, а 2 - й слой из электролита, содержащего серу в составе органических добавок. Потенциал никеля, содержащего серу, имеет более отрицательное значение, чем потенциал никеля без включений серы. Поэтому второй слой электрохимически защищает от коррозии первый слой никеля. Таким образом обеспечивается более высокая защита основного изделия. [30]
Страницы: 1 2 3