Потенциал - никель
Cтраница 3
Наиболее эффективными являются многослойные ( 2 - 3 слоя) никелевые покрытия, защитная способность которых намного выше однослойных. Характерны двух-и трехслойные покрытия никелем, в которых сочетаются первый слой, не содержащий серы, и последующие слои с включением различного количества серы. Так как потенциал никеля, содержащего серу, имеет более отрицательное значение, чем у никеля без включения серы, то второй слой электрохимически ( анодно) защищает от коррозии первый слой никеля и таким образом обеспечивается более высокая защитная способность покрытия в целом. [31]
Никелирование относится к группе катодных покрытий, поэтому надежная защита возможна только при минимальной пористости соединения. Для повышения защитных свойств применяют многослойные покрытия медь-никель или никель-медь-никель. Так как разница в потенциалах никеля и стали не велика, то при увеличении толщины никелевого покрытия допускается его применение как однослойного для деталей приборов, работающих в легких условиях эксплуатации. Твердость никелевых покрытий ниже твердости хромовых, но приближается к твердости закаленных сталей. Покрытие допускает изгибы, запрессовку, однако возможны случаи отслаивания при расклепке и развальцовке. Стойкость при трении значительно выше, чем у цинкового покрытия. Покрытие хорошо противостоит действию растворов щелочей и слабых кислот. [32]
Многослойные в два-три слоя никелевые покрытия обладают большей коррозионной стойкостью, чем однослойные. Первый слой никеля осаждают из простого никелевого электролита, а 2 - й слой из электролита, содержащего серу в составе органических добавок. Потенциал никеля, содержащего серу, имеет более отрицательное значение, чем потенциал никеля без включений серы. Поэтому второй слой электрохимически защищает от коррозии первый слой никеля. Таким образом обеспечивается более высокая защита основного изделия. [33]
Стандартные потенциалы олова и никеля различаются примерно на 0 1 В, причем потенциал никеля отрицательнее потенциала олова. Катодная поляризация при электролизе растворов солей ( сульфатов, хлоридов) выражена значительно резче для никеля, чем для олова. Если же к хлоридному электролиту добавить фторид натрия или аммония, то стационарные и катодные потенциалы выделения олова приобретают более отрицательные значения, чем потенциалы никеля в таком же растворе. [34]
Стандартные электродные потенциалы железа, кобальта и никеля в водной среде при температуре 25 С составляют соответственно - 0 44; - 0 277 и - 0 250 В. Очевидно, что металлы, более электроположительные, чем основной металл сплава, будут включаться в катодный осадок. При совместном разряде ионов Fe2, Co2, № 2 в сплав могут входить и металлы, более электроотрицательные, чем основной металл. Так, потенциал никеля при значениях силы тока, применяемых в гальванопластике, значительно сдвинут в отрицательную сторону. В работе [50] подробно рассмотрена кинетика включения примесей металлов в сплав. [35]
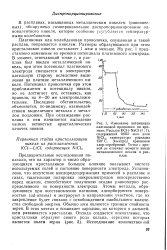
На рис. 1 показано влияние атомарного водорода на потенциал никеля в 1 TV NaOH без пропускания электрического тока. По оси абсцисс отложено время в минутах; по оси ординат - потенциал электрода в вольтах против обратимого водородного электрода. Как видно из хода кривой ( рис. 1), в начале опыта потенциал электрода был на 550 мв по-ложительнее водородного. Под действием Н - атомов потенциал никеля постепенно сдвигался в отрицательную сторону и через 20 мин. [36]
Осажденные металлы легко отделяют от покрытой свинцом поверхности цилиндров. Снятый лист нарезают на квадратики, соответствующие размерам лепестков, которые далее обрабатывают для удаления меди. При нагревании и интенсивном перемешивании на них действуют соответствующей жидкостью, растворяющей медь. Важно, чтобы в применяемом растворе потенциал меди был более отрицателен, чем потенциал никеля; тогда медь в короткозамкнутом элементе Ni раствор Си работает как растворимый анод. [37]
При погружении в кислый раствор соли никеля изделий из цинка и его сплавов происходит взаимное вытеснение никеля цинком вследствие различных их потенциалов, по уравнению реакции Zn - f - NiSO4ZnSO4 Ni. Пленка никеля неплотно пристает к поверхности, легко отслаивается вместе с электролитическим осадком никеля, а раствор загрязняется цинком, который резко ухудшает качество никелевого покрытия. Поэтому при непосредственном никелировании изделий из цинка и его сплавов очень важно, чтобы потенциал катода достигал значений выше стационарного потенциала цинка в никелевом растворе. Это осуществляют добавлением к никелевому электролиту лимонной, винной, фосфорной кислот или их солей ( около 1 г-экв / л), образующих комплексные соединения с никелем и тем самым смещающих потенциалы никеля в сторону более отрицательных значений. На практике при никелировании изделий из цинкового сплава, содержащего около 4 % А1 ( литье под давлением) чаще применяют предварительное меднение из цианистого электролита, так как добавление указанных выше кислот или их солей не всегда приводит к положительным результатам. [38]
Для металлов второй группы характерна другая форма кривой поляризации [21]: поляризация при электролизе не уменьшается и при перерыве тока на различные промежутки времени она практически остается постоянной. Постоянство поляризации при различной продолжительности; перерыва не означает отсутствия пассивирования, а наоборот, указывает на его большую скорость, поскольку склонность этих металлов к пассивированию значительно больше, чем металлов первой группы. Действительно, в работе Гекстра [22] было показано, что при разрушении соскабливанием пассивной пленки с поверхности катода при осаждении никеля потенциал последнего смещается в более отрицательную сторону. В одной из наших предыдущих работ также было установлено, что при снятии поляризационной кривой никеля [23] быстрым методом потенциал без тока тем отрицательнее, чем больше скорость снятия кривой. Смещение потенциала свежеосажденного никеля в более положительную сторону связано с пассивированием поверхности металла. В результате этого она пассивируется, переходя в более устойчивое состояние. Скорость же перехода в более устойчивое состояние, как уже отмечалось, различна в зависимости от условий электролиза и природы осаждаемого металла. В связи с наличием на поверхности катода прочной пленки из чужеродных частиц ( для металлов второй группы) значительная часть перенапряжения обусловлена затруднением разряда ионов металла адсорбированными на поверхности электрода чужеродными частицами. [39]
Платиновая или молибденовая проволочка, опущенная в такой расплав, покрывается никелем. Размеры образующихся при этом кристалликов никеля составляет 1 мкм и меньше. На рис. 1 представлено изменение во времени потенциала платинового электрода. В момент, отвечающий точке с, в расплав был введен металлический никель, при этом потенциал платинового электрода смещается в электроотрицательную сторону вследствие выделения на платине металлического никеля. Потенциал проволочки при этом приближается к потенциалу никеля, но не достигает его, оставаясь, как правило, на 8 - 20 мв электроположи-тельнее. Последнее обстоятельство, объясняется, по-видимому, взаимодействием выделяемого металла с металлом подложки. При охлаждении расплава в нем начинается выпадение мелких ветвистых кристаллических цепочек никеля. [41]
Интересные сведения можно получить также при изучении катодной поляризации никеля методом быстрого снятия кривых, когда катодная поляризация чередуется с анодной. В этом случае катодная ветвь, следующая после анодной, может иметь искаженную форму в результате изменения состояния поверхности электрода в анодном периоде. На рис. 29 показаны такие поляризационные кривые, снятые при скорости 7 5 сек. Из приведенного рисунка видно, что кривые имеют довольно сложную форму; поэтому для лучшего понимания их сущности рассмотрим рис. 29 более подробно. Положение сплошной горизонтальной линии соответствует стационарному потенциалу никелевого электрода в изучаемом растворе до начала электролиза, а пунктирная линия характеризует потенциал электрода сравнения, по отношению к которому можно определить потенциал никеля. В точке а на ячейку подается ток. После достижения максимума анодная поляризация уменьшается и в точке в изучаемый электрод поляризуется катодно. Однако, как видно из рис. 29, потенциал электрода задерживается некоторое время в анодной области, образуя небольшую ступеньку, после чего он резко смещается в катодную область. После некоторой задержки потенциал катода достигает максимума в точке с и начинает уменьшаться вследствие умень шения катодного тока. Нисходящая ветвь катодной кривой имеет неискаженную форму. В точке d ток и, соответственно, поляризация проходят через нуль, и вновь начинается анодный цикл. После окончания анодного цикла в точке е, когда уже началась катодная поляризация электрода, потенциал опять задерживается в анодной области, причем в этом случае продолжительность задержки больше, чем в первый раз. Однако потенциал, при котором происходит задержка, такой же, как и в первом случае. Затем ход кривой повторяется, как уже было описано. После третьего и четвертого анодных периодов продолжительность задержки потенциала в анодной области при катодной поляризации электрода еще больше, но она происходит каждый раз при одном и том же потенциале. Постоянство потенциала, отри котором наблюдается задержка, свидетельствует о том, что при этом происходит восстановительный процесс, связанный с фазовыми превращениями. [42]
Электролитическое выделение никеля и других металлов группы железа сопровождается значительной анодной и катодной поляризацией. В сильнокислых средах выделение никеля на катоде почти невозможно, поскольку на нем выделяется почти один нодород. В растворах с небольшой кислотностью, близких к iicii - ральным, изменение рН резко сказывается на работе электролита, причем изменяются как свойства никелевых осадков, так и выход металла по току. Чрезвычайно важную роль играет также режим работы никелевых электролитов, так как катодная плотность тока, температура электролита и перемешивание значительно влияют на величину поляризации и на структуру осаждаемых никелевых осадков. Значение рН электролита, концентрация никеля и режим никелирования должны быть тесно увязаны друг с другом. Определяя оптимальную кислотность никелевого электролита, необходимо учитывать два обстоятельства: 1) при недостаточном содержании ионов водорода в электролите ( рН выше 6 3) образуется гидроокись никеля и осадки делаются темными; 2) при уменьшении значения рН электролита ( ниже 4) количество водорода, выделившегося на катоде, будет значительно увеличиваться, гак как потенциал никеля электроотрицательнее потенциала водорода, что вызовет резкое снижение выхода металла по току и ухудшит сцепление осадка с покрываемой поверхностью. [43]
Страницы: 1 2 3