Потенциал - пробой
Cтраница 1
 |
Влияние кислого углекислого кальция на коррозию алюминия. [1] |
Потенциал пробоя смещается в положительную сторону с уменьшением концентрации ионов хлора. Если в воде содержатся соли лимонной кислоты, скорость коррозии алюминия, как указывает Троцтнер [111,192], увеличивается, что объясняется образованием комплексных соединений, растворимых в воде. [2]
Потенциал пробоя нелегированного циркония, выплавленного из циркониевой губки, полученной по методу Кролла, быстро достигается при экспозиции в паре или горячей воде при рабочих температурах реакторов. Еще в ранних исследованиях, проведенных в США, было установлено, что такое поведение объясняется почти неизбежным присутствием в металле азота, вредное воздействие которого можно компенсировать введением добавок олова [71] - так был создан сплав Циркалои 2, содержащий примерно 1 5 % Sn, 0 1 % Fe, 0 1 % Сг и 0 05 % Ni, предназначенный для водоохлаж-даемых реакторов. Известно, однако, что даже в случае применения этого сплава на стойкость конструкции оказывают влияние технологические операции обработки материала в ходе его изготовления. По этой причине используется строгая система коррозионных испытаний [72, 73], назначение которой - подтвердить сохранение высокой коррозионной стойкости заготовок и конечной продукции. Материал удовлетворительного качества после таких испытаний имеет прирост массы 28 10 мг / дм2 и покрыт глянцевой черной пленкой. Неудовлетворительное качество материала обнаруживает себя высоким значением прироста массы ( достигающим 100 мг / дм2), а также внешним видом поверхностной пленки, состоящей из белого продукта коррозии. [3]
Потенциал пробоя пассивной пленки в присутствии иона-активатора зависит от природы металла. Поэтому в присутствии ионов-активаторов одного и того же вида и той же концентрации один металл может подвергаться питтинговой коррозии, а другой нет. [4]
Определены потенциалы пробоя покрытий, коррозионные токи различных гальванопар, проведена сравнительная оценка электрохимических параметров для ВТ -, ВДО - и ТО-образцов, выявлено влияние природы электролита на электрохимическое поведение образцов. [5]
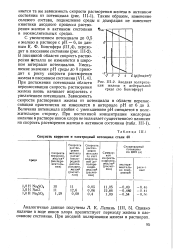
Зависимость потенциала пробоя ( кривая А) и механической прочности связи ( кривая Б) от концентрации KF ( I) и NaF ( II) при выделении осадков цинка и никеля на алюминии при 25 С. [6]
Зависимость потенциала пробоя ( кривая А) и механической прочности связи ( кривая Б) от плотности тока при выделении осадков цинка и никеля на алюминиевую подложку при 25 С. [7]
 |
Скорость коррозии и электродный потенциал стали 40.| Анодная поляризация железа в нейтральной среде ( по Бонгоферу. [8] |
Величина потенциала пробоя с уменьшением рН смещается в полс-жительную сторону. [9]
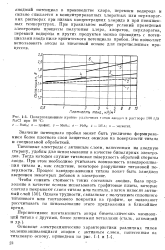 |
Поляризационные кривые различных типов анодов в растворе 300 г / л. [10] |
Значение потенциала пробоя может быть увеличено формированием более плотного слоя защитных окислов на поверхности титана и специальной обработкой. [11]
Сравнение потенциалов пробоя различных фторуглеродов с потенциалом пробоя гексафторида серы и азота показывают, что C3F8, C4F10 и CSP12 в газообразном состоянии не только не уступают гексафториду серы по своей изолирующей способности, но даже превосходят его и что все без исключения фторуглероды являются лучшими диэлектриками, чем азот. [12]
После достижения потенциала пробоя электрод из германия электронной проводимости покрывается мелкими ямками, в которых, по-видимому, только и развивается пробой. В концентрированных растворах пробой не наступает, так как образующиеся ямки заполняются плохо растворимыми продуктами анодной реакции. Этим также можно объяснить быстрое повышение потенциала при высоких плотностях тока в 0 1 N растворе H2SO4, как показано на фиг. [13]
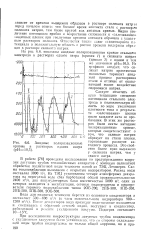 |
Анодные поляризационные кривые в растворах едкого натра ( рН Ю 5. [14] |
Видно увеличение потенциала пробоя и возрастание склонности к залечиванию защитных пленок при увеличении времени контакта образцов с указанным раствором силиката. Отмечается также сдвиг стационарного потенциала в положительную область с ростом времени выдержки образцов в растворе силиката натрия. [15]
Страницы: 1 2 3 4