Потенциал - окислительно-восстановительная система
Cтраница 3
Кроме того, факторы, влияющие на потенциал, в свою очередь зависят от температуры, как, например, коэффициент активности. Особенно велико влияние температуры на потенциал окислительно-восстановительных систем, включающих гетерогенную фазу. [31]
Окислительно-восстановительные потенциалы биологических систем представляют большой интерес. Последовательность окислительных реакций в организме определяется уровнями потенциалов окислительно-восстановительных систем. [32]
Термодинамическая возможность данного процесса сводится к требованию, чтобы потенциал окислительно-восстановительной системы был более отрицателен, нежели потенциал равновесного водородного электрода в данном растворе. [33]
Термодинамическая возможность данного процесса сводится к тому, чтобы потенциал окислительно-восстановительной системы был более отрицателен, нежели потенциал равновесного водородного электрода в данном растворе. [34]
Однако если выбрать одну из окислительно-восстановительных систем в качестве стандартной, то относительно нее становится возможным измерение потенциала любой другой окислительно-восстановительной системы независимо от выбранного индифферентного электрода. Нг 1 013 - 103 гПа ( 1 атм) и ан 1 моль / л при любой температуре ] принят равным нулю. [35]
Используют кривые окислительно-восстановительного титрования, в частности перманганатометрического титрования. Но если кривые кислотно-основного титрования показывают зависимость степени от-титрованности от рН раствора, то кривые перманганатометрического титрования выражают зависимость потенциала окислительно-восстановительной системы от степени оттитрованное, вблизи точки эквивалентности происходит резкий скачок редокс-потенциала ( см. гл. [36]
Для сравнения потенциалов между собой берут отношение [ окисл. Величины окислительно-восстановительных потенциалов измеряют по отношению к нормальному водородному электроду. Потенциал окислительно-восстановительной системы, измеренный по отношению к обратимому водородному электроду, принятому за нуль, при условии, когда отношение концентраций окисленной и восстановленной форм равно единице, называется нормальным окислительно-восстановительным потенциалом. Знак означает, что электроны движутся от водородного электрода. [37]
Вещество окисляется, если теряет электроны или одновременно электроны и протоны ( водородные атомы, дегидрирование), или присоединяет кислород. Редокс-потенциал определяют путем измерения электродвижущей силы в вольтах. Чем меньше потенциал окислительно-восстановительной системы, тем легче она отдает электроны и в большей степени является восстановителем. Чем выше потенциал системы, тем сильнее выражены ее окислительные свойства, т.е. способность принимать электроны присуща только молекулам с более высоким редокс-потенциалом. Это правило лежит в основе последовательности расположения промежуточных переносчиков электронов от водородов субстратов до кислорода. [38]
Из-за разнообразия используемого оборудования, первичного сырья, вторичных отходов и возникающих трудностей по оценке его эффективности, качеству и экологическим показателям получаемых материалов, задача исследования энергетической неоднородности имеет большое значение. Для исследования неоднородности поверхности применяется потенциометрическая методика определения адсорбции гидроксоаквакомплексов Fe ( III) из водных растворов. Методика заключается в измерении потенциала окислительно-восстановительной системы Fe2 - Fe3 в водной суспензии, в которой устанавливается равновесие между концентрацией ионов Fe3 в растворе и на поверхности дисперсного материала. [39]
В реальных условиях в ряде случаев значения нормальных потенциалов не могут служить для сравнения поведения систем. Fe ( CN) g - и потенциал окислительно-восстановительной системы изменяется до - - 0 36 В. [40]
Определение констант нестойкости потенциометрическим методом, как отмечают в ряде статей К. Б. Яцимирский [1] и Н. П. Комарь [2], может быть осуществлено при изучении зависимости потенциала окислительно-восстановительных систем от концентрации комплексообразователей. Здесь, однако, необходимо учитывать, что в нейтральной среде ( или в слабокислой или слабощелочной за счет гидролиза) многие катионы находятся в форме сложных ионов или в форме нерастворимых соединений. Кроме того, электропроводность сантинормальных водных растворов мала и измерение потенциала окислительно-восстановительных систем, особенно до введения комплексо-образователя, не всегда возможно. Следовательно, определение константы нестойкости потенциометрическим методом возможно лишь в том случае, если измерение потенциала окислительно-восстановительных систем производят при различной концентрации комплексообразователя. Отметим, что, согласно литературным данным, большинство ионов образует с одним аддендом несколько комплексов. [41]
Применение ртутного электрода [77] ограничено узким интервалом потенциалов, при которых электрод индифферентен. В некоторых системах и главным образом для целей потенциометрического титрования применяют графитовые электроды. Стеклянные полупроводниковые электроды с электронной функцией не чувствительны к кислородной системе и поэтому позволяют измерять потенциал окислительно-восстановительной системы в условиях аэрации. [42]
Определение констант нестойкости потенциометрическим методом, как отмечают в ряде статей К. Б. Яцимирский [1] и Н. П. Комарь [2], может быть осуществлено при изучении зависимости потенциала окислительно-восстановительных систем от концентрации комплексообразователей. Здесь, однако, необходимо учитывать, что в нейтральной среде ( или в слабокислой или слабощелочной за счет гидролиза) многие катионы находятся в форме сложных ионов или в форме нерастворимых соединений. Кроме того, электропроводность сантинормальных водных растворов мала и измерение потенциала окислительно-восстановительных систем, особенно до введения комплексо-образователя, не всегда возможно. Следовательно, определение константы нестойкости потенциометрическим методом возможно лишь в том случае, если измерение потенциала окислительно-восстановительных систем производят при различной концентрации комплексообразователя. Отметим, что, согласно литературным данным, большинство ионов образует с одним аддендом несколько комплексов. [43]
В любом процессе титрования изменяется концентрация реагирующих веществ, иначе говоря, степень оттитрованности / ( см. гл. Графическое изображение изменения рН в процессе титрования представляет собой кривую титрования для кислотно-основного взаимодействия. Если перейти к методам окислительно-восстановительного титрования и взять за независимую переменную степень оттитрованности, то зависимой переменной в этом случае будет потенциал окислительно-восстановительной системы, находимый по формуле Нернста ( см. гл. [44]
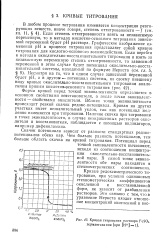 |
Кривая титрования раствора FeSC4 перманганатом ( при [ Н ] l. [45] |
Страницы: 1 2 3 4