Потенциал - водородный электрод
Cтраница 1
Потенциал водородного электрода, конечно, зависит от температуры. [1]
Потенциал водородного электрода воспроизводится с очень высокой точностью. Поэтому водородный электрод и принят в качестве эталона при создании шкалы электродных потенциалов. [2]
Потенциал водородного электрода зависит от температуры, концентрации ионов водорода ( более правильно - активности) в растворе и давления водорода на поверхности электрода. Эти параметры следует определять с особой тщательностью, чтобы данная полуреакция служила в качестве эталона. [3]
Потенциал водородного электрода для концентрации 1 г-ион / л и давлении РНг, равном 1 am, называется нормальным и принят равным нулю. [4]
Потенциал водородного электрода, конечно, зависит от температуры. [5]
Потенциал водородного электрода, конечно, зависит от температуры. Эту зависимость можно было бы установить, если бы существовал какой-то другой электрод, для которого она была бы известна. Но в этом отношении любой электрод ничем не отличается от водородного. Измерения потенциалов различных электродов по водородному должны производиться в условиях, когда оба электрода находятся при одной и - той же температуре. [6]
Потенциал водородного электрода воспроизводится с очень вы сокой точностью. Поэтому водородный электрод и принят в качестве эталона при создании шкалы электродных потенциалов. [7]
 |
Водородный электрод. [8] |
Потенциал водородного электрода воспроизводится с очень высокой точностью. Поэтому водородный электрод и принят в качестве эталона при создании шкалы электродных потенциалов. [9]
Потенциал водородного электрода, погруженного в раствор с активностью ионов водорода, равной единице, и при парциальном давлении водорода в газовой фазе равном единице, называется нормальным потенциалом и условно принят за нуль шкалы потенциалов. Такой электрод является электродом сравнения. Измеренная разность потенциалов между двумя электродами - нормальным водородным и нормальным испытуемым - равна величине нормального потенциала испытуемого электрода. [10]
Потенциал водородного электрода условно принят равным нулю. Работа с ним сопряжена с ря - дом неудобств, но он имеет большое значение как эталонный электрод. [11]
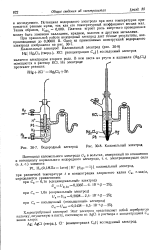 |
Водородный электрод [ IMAGE ] - 8. Каломельный электрод. [12] |
Потенциал водородного электрода при всех температурах принимается равным нулю, так как его температурный коэффициент весьма мал. [13]
Потенциал водородного электрода устанавливается сравнительно медленно. Электрод чувствителен к ядам ( As, Se, H2S и др.), присутствующим как в электролите, так ив качестве примесей к газообразному водороду, которым насыщается платина. Это ограничивает возможности применения водородного электрода при различных электрохимических измерениях. [14]
Потенциал водородного электрода о, измеренный против какого либо стандартного электрода, дает возможность судить о степени действительной кислотности ( рН) того раствора, в который данный водородный электрод погружен. [15]
Страницы: 1 2 3 4