Электронный потенциал
Cтраница 2
Сопоставляя данные, приведенные в табл. 4.3, с такими характеристиками металлов, как первый потенциал ионизации, работа выхода электрона, радиус иона, электроотрицательность, сродство к электронам и стандартный электронный потенциал в водных растворах, можно прогнозировать энергетические взаимодействия активных групп маслорастворимых ПАВ и металлов, а также ориентировочно оценивать дипольный момент и относительную степень ионности металлсодержащих маслорастворимых ПАВ. [16]
Электрохимическая коррозия - это взаимодействие материала с коррозионной средой ( растворы электролита), при котором ионизация атомов материала и восстановление окислительной компоненты протекают не в одном акте и их скорости зависят от электронного потенциала материала. [17]
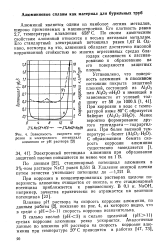 |
Зависимость скорости кор. [18] |
Менее вероятно формирование другого тригидрата - гидраргил-лита. Электронный потенциал алюминия при образовании защитной пленки повышается не менее чем на 1 В. [19]
Множитель i указывает на то, что V ( r) сдвинуто по фазе на 90 относительно вектора смещения в той же точке. Такой электронный потенциал, возникающий из-за наличия фононов в кристалле, называется электрок-фононным взаимодействием. Мы видели, что свободные электроны & кристалле могут быть созданы либо введением примесей, либо тепловым возбуждением идеального кристалла. Такие свободные электроны дают вклад в электропроводность, однако про водим ость будет ограничиваться рассеянием электронов на колебаниях решетки или дефектах. Мы не будем подробно останавливаться на теории явлений переноса, и в частности на электропроводности; эти вопросы рассматриваются в большинстве учебников по физике твердого тела. Однако мы исследуем природу таких явлений в кристаллах как электрон-фоно нное взаимодействие, которое входит в указанную выше теорию. [20]
Разбавленные кислоты действуют на олово очень медленно. Это связано с близостью стандартных электронных потенциалов Sn и Н2 ( гл. В концентрированной соляной кислоте, в особенности при нагревании, олово растворяется легко. [21]
 |
Схемы кристаллических решеток. [22] |
Анизотропия характерна и для поверхностных слоев кристаллов. Такие свойства как поверхностное натяжение, электронные потенциалы, адсорбционная способность, химическая активность существенно различны у различных граней кристаллов. [23]
Очевидно, что материалу под нагрузкой присущи иные физические и физико-химические свойства, чем ненагруженному. Это проявляется, в частности, в пониженном электронном потенциале и в меньшей коррозионной стойкости упругонапряженных и наклепанных металлов. [24]
Альдегиды восстанавливаются несколько легче, чем кетоны. Восстановление карбонильной группы до одноатомного спирта обычно требует меньшего электронного потенциала, чем восстановление до пинакона. В большинстве случаев для получения более восстановленной формы - углеводорода - применяют так называемые каталитические электроды. Наиболее пригоден для этой цели кадмиевый электрод. [25]
Возникшая вследствие тех или иных факторов электрохимическая неоднородность является причиной разделения поверхности на катодные и анодные участки. При этом участки с более отрицательным электродным потенциалом образуют аноды, я участки, имеющие более положительный электронный потенциал, образуют катоды. На анодных участках ион-атомы металла могуч переходить в раствор и освобождать электроны, а усвоение свободных электронов частицами раствора происходит на катодных участках поверхности раздела металл - электролит. [26]
Свобода азимутальных поворотов, как говорилось выше, дает право аппроксимировать молекулу цилиндром. При пересечении цилиндров с плоскостью, перпендикулярной осям молекул, получаются концентрические пояса - области повышенной плотности электронного потенциала. Следовательно, где-то в области пересечения сферы интегрирования с центральным цилиндром должен выявиться межмолекулярный максимум. [27]
По-видимому, активность металлов цериевой подгруппы и инертность металлов иттриевой подгруппы ( несмотря на близкие значения их электронных потенциалов) связаны с различиями в кинетических характеристиках процесса взаимодействия с водой. Возможно, что легкие лантаниды более реакционноспособны из-за большей координационной ненасыщенности вследствие их большего, чем у иттриевых РЗЭ, радиуса атомов. [28]
В связи с проблемой водородных состояний в a - Si: Н особенный интерес представляют электронные свойства a - Si, а именно хвосты плотности состояний и поведение электронов в хвостах. В зтих теориях используется модель модифицированного беспорядка размещения и предположение о конечности возмущения ( обусловленного связью Si-H) в электронном потенциале матрицы чистого Si. [29]
Представлены основные электронные ресурсы ГОПБ, которые до сих пор не были известны широкой библиотечной общественности в силу специфики и особенностей работы названной библиотеки. Будет сделано подробное описание существующих информационных массивов с учетом их развития и использования, а так же даны перспективы дальнейшей работы по созданию и организации доступа к электронным коллекциям документов ГОПБ, отражающим ее богатейшие книжные собрания. При рассмотрении существующего и создающегося электронного потенциала библиотеки будет также проанализировано программное обеспечение, технологии и пути реализации различных проектов, с помощью которых создавались электронные ресурсы ГОПБ. [30]
Страницы: 1 2 3