Стационарный потенциал
Cтраница 2
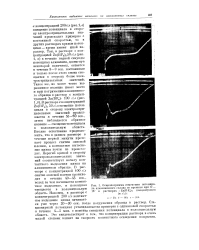 |
Осциллограммы изменения потенциала алюминиевого сплава во времени при 17 - 18 в растворах. з Zn ( BF4 2 концентрации. [16] |
Стационарный потенциал устанавливается примерно с одинаковой скоростью в течение 4 - 5 мин. Это свидетельствует о том, что концентрация раствора в очень малой степени влияет на скорость контактного осаждения покрытия. [17]
 |
Зависимость скоростей реакций разряда и ионизации водо. [18] |
Стационарный потенциал определяется взаимным расположением поляризационных кривых парциальных процессов. Так как скорости отдельных процессов зависят от состояния поверхности электрода, то Ес также является функцией состояния поверхности металла в отличие от равновесного потенциала. Равновесный потенциал водородного электрода не зависит от природы металла. [19]
Стационарный потенциал - потенциал металлического сооружения, измеренный относительно электрода сравнения при отсутствии блуждающих токов, поляризации от внешних источников тока. [20]
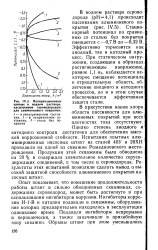 |
Поляризационные кривые в водном растворе, насыщенном сероводородом, для алюминиевого покрытия. [21] |
Стационарный потенциал по сравнению со сталью без покрытия смещается с - 0 7 В до - 0 32 В. Эффективно тормозится как анодный, так и катодный процесс. При статическом нагру-жении, создающем в образцах растягивающее напряжение, равное 1 1 От, наблюдается некоторое смещение потенциала в отрицательную область, облегчение анодного и катодного процессов, но и в этом случае обеспечивается эффективная защита стали. [22]
Стационарный потенциал, который устанавливается на границе металл - раствор, отличается от равновесных потенциалов водорода и металла. [23]
Стационарный потенциал, измеренный на титане в концентрированных растворах щелочи, намного отрицательнее, чем в растворах кислот, и составляет величину порядка - 1 3 в. Скорость коррозии в 30 % - ном растворе КОН при 100 С практически равна нулю, тогда как в 40 % - ном растворе она составляет уже 0 4 г / м2 - час. Следовательно, при 100 С предельная концентрация щелочи, до которой титан может быть использован без опасения больших коррозионных потерь, составляет 30 вес. [24]
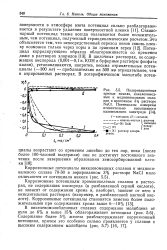 |
Поляризационные кривые никеля, никелевомед-ных и медноникелевых сплавов в проточном 3 % растворе NaCl. Потенциалы измерены относительно насыщенного каломельного электрода. [25] |
Стационарный потенциал также всегда оказывается более положительным, чем потенциал, полученный термодинамическим расчетом. КОН и буферные растворы фосфата калия), устанавливаются, напротив, весьма отрицательные потенциалы ( - 300 мв) - приблизительно на 500 мв отрицательнее, чем в аэрированных растворах. [26]
Стационарные потенциалы даны через 6 час испытаний. Скорость коррозии рассчитана по привесу образцов. [27]
Стационарный потенциал регистрируется относительно хлорсе-ребря н ого электрода сравнения. [28]
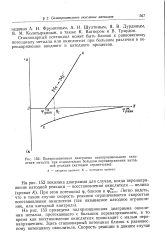 |
Поляризационная диаграмма самопроизвольного окисления металла при относительно большом перенапряжении катодной реакции ( катодное ограничение. [29] |
Стационарный потенциал может быть близок к равновесному потенциалу металла или окислителя при большом различии в перенапряжении анодного и катодного процессов. [30]
Страницы: 1 2 3 4 5