Стационарный потенциал - титан
Cтраница 1
Стационарный потенциал титана в 40 % - ном растворе серной кислоты, содержащем 0.3 М ионов Т1, при 100 С. [1]
Стационарные потенциалы титана без контакта и в контакте с латунью, железом и цинком в 6 % - ном растворе NaCl с рН 6 при 100 С равны соответственно: - 0 35 В; - 0 5 В; - 0 8 В и - 1 1 В. [2]
Достаточно положительный стационарный потенциал титана, при котором основным катодным процессом является восстановление добавляемого в электролит окислителя; катодный ток за счет реакции восстановления водорода незначителен или полностью отсутствует, что существенно снижает или исключает наводороживание титана и его сплавов. [3]
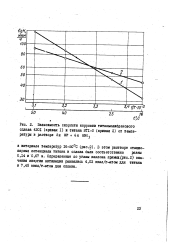 |
Зависимость скорости коррозии титанмолибденового сплава 4201 ( кривая I и титана BTI-0 ( кривая 2 от температуры в растворе 2н HP 6 я. [4] |
В этом растворе стационарные потенциалы титана и сплава были соответственно равны 0 14 и 0 67 в. Определенные до углам наклона прямых ( рис. 2) значения энергии активации равнялись 4 02 ккад / г-атом для титана и 7 45 ккал / г-атом для сплава. [5]
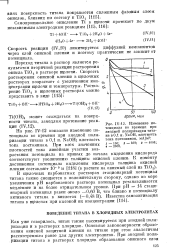 |
Изменение потенциала во времени при анодной поляризации титана в 0 1 н. NaOH, плотность тока постоянная, мА / м2. [6] |
В щелочных карбонатных растворах стационарный потенциал титана также смещается в положительную сторону, однако по мере увеличения рН карбонатного раствора потенциал устанавливается медленнее и на более отрицательном уровне. [7]
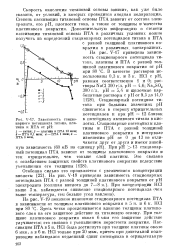 |
Зависимость стационарного потенциала титана, платины и ПТА от рН. [8] |
На рис. V-17 приведена зависимость стационарного потенциала титана, платины и ПТА с разной толщиной платинового покрытия от рН при 80 С. Стационарный потенциал титана при больших значениях рН сдвигается в сторону отрицательных потенциалов и при рН 12 близок к потенциалу активного титана в кислотах. При рН 13 стационарный потенциал ПТА зависит от толщины платинового покрытия и тем отрицательнее, чем тоньше слой платины. [9]
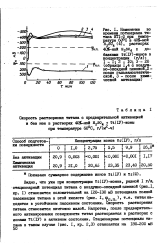
В табл. 3 показано, как изменяется стационарный потенциал титана в зависимости от изменения температуры в 40 % - ном растворе серной кислоты при концентрации 0 3 М ионов четырехвалентного титана. Из данных таблицы видно, что по мере повышения температуры стационарный потенциал титана облагораживается от значения 0 485 в при 0 С до 0 675 в при 100 С, что указывает на повышение защитных свойств пленки. [10]
Кривая 6 па рис. 7 изображает зависимость стационарных потенциалов титана, хрома, платины и сплавов титана с хромом в 57 % - ной азотной кислоте при 100 С. При увеличении содержания хрома в сплаве потенциал становится все более положительным, что, по-видимому, связано с изменениями в полупроводниковых свойствах окисных пленок, возникающих на поверхности титана и его сплавов. [11]
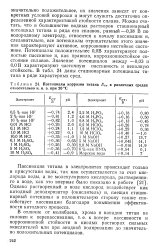 |
Потенциалы коррозии титана Ест в различных средах относительно н. в. э. при 20 С. [12] |
Можно считать, что в большинстве водных растворов стационарный потенциал титана и ряда его сплавов, равный - 0 38 В по водородному электроду, относится к началу пассивации и, следовательно, все потенциалы отрицательнее этого значения характеризуют активное, коррозионно нестойкое состояние. Потенциалы положительнее 0 0В характеризует полностью пассивное и, как правило, коррозионностойкое состояние сплавов. Значение потенциалов между - 0 03 и 0 0 В характеризуют частичную пассивность и неполную стойкость. В табл. 24 даны стационарные потенциалы титана в ряде характерных сред. [13]
 |
Изменение во времени потенциала титана BTI-0 при темпе60 С в 4056-ной. [14] |
Видно, что уже при концентрации т ( 1У) - ионов, равной I г / л, стационарный потенциал титана с воздушно-оксидной пленкой ( рис. 1, кр. I) становится положительней на 120 - 130 мВ потенциала полной пассивации титана в этой кислоте ( рис. I, tpn. Скорость растворения титана становится ничтожно малой. Напротив, после предварительного активирования поверхности титан растворяется в растворах с ионами Т1 ( 1У) в активном состоянии. [15]
Страницы: 1 2 3