Стационарный потенциал - титан
Cтраница 3
Примерно такие же соотношения между анидным и катодным контролем получаются и в 10 % - ной серной кислоте. В более концентрированных кислотах доля катодного торможения будет несколько возрастать, так как стационарный потенциал титана при повышении концентрации кислоты немного сдвигается в отрицательную сторону, а нормальный потенциал водородного электрода - в положительную. Таким образом, несмотря на то, что титан в растворах серной и соляной кислот концентраций выше 10 % находится в активном состоянии, он корродирует с преобладающим анодным контролем. Это является прямым указанием на то, что в этих условиях мы все же имеем титан не полностью в активном состоянии, а лишь в состоянии частичной пассивности. [31]
Интересная работа выполнена коллективом авторов [87], изучавших возможность анодной защиты титана при получении хлората хрома, основанном на растворении его гидрокси-да соляной кислотой. При введении в раствор совместно с хлоратом хлорида хрома ( сильного восстановителя) стационарный потенциал титана сдвигается в сторону отрицательных значений от 0 6 до - 0 12 В. [32]
Если принять за начальный потенциал анодного процесса нормальный потенциал реакции Ti - Ti3 Зе равный - 1 21 в ( см., например, [15]), а за начальный потенциал катодного процесса нормальный потенциал водородного электрода, считая его в 10 % - ной H. В серной кислоте более высоких концентраций доля катодного торможения будет несколько возрастать, так как стационарный потенциал титана при повышении концентрации кислоты немного сдвигается в отрицательную сторону, а нормальный потенциал водородного электрода - в положительную. [33]
При исследовании поляризации сплавов титана с платиной и палладием в соляной кислоте получены аналогичные кривые с приведенными на фиг. Стационарные потенциалы сплавов вследствие снижения перенапряжения водорода оказываются сильно сдвинутыми в положительную сторону по сравнению со стационарным потенциалом титана, так, что, например, в соляной кислоте до 20 % - ной концентрации потенциалы сплавов оказываются в области устойчивого пассивного состояния. [34]
Электрохимические свойства титановых сплавов определяются преимущественно свойствами их главного компонента - титана. Равновесный электрохимический потенциал титана по отношению к водородному электроду равен - 1 63 В, что свидетельствует о его высокой термодинамической активности. Стационарные потенциалы титана в большинстве водных сред намного положи-тельнее; в морской воде при 25 С этот потенциал равен 0 09 В [177], что указывает на меньшую электрохимическую активность титана в данных условиях по сравнению с железом и на высокую стойкость его пассивного состояния. [35]
Как видно из кривых ( рис. 1), для сплавов титана петли активного анодного растворения, свидетельствующей о возможности активации металла, не обнаружено. Для титана же такая петля появляется в растворах с 20, 15 и 10 % НС. Стационарный потенциал титана в растворах с 20 - 10 % НС1 находится в области активного растворения, с 5 % НС1 - в пассивной области. По значениям увеличивающихся токов металлы располагаются в следующем порядке: Ti-Mo; Ti-Pd и Ti. У сплавов Ti-Mo в области положительных потенциалов наблюдается увеличение тока. По-видимому, это вызвано молибденом, так как в данных условиях он имеет повышенную скорость растворения за счет перепассивации. [36]
Аналогичный эффект наблюдается при легировании титана палладием. Как показали результаты коррозионных испытаний, скорость коррозии сплава Ti с 1 % Pd в 40 % - ной H2S04 составляет 0 01 г / м2 - час при 25 С и 0 57 г / м2 час - при 50 С, в то время как для нелегированного титана скорость коррозии равна соответственно 2 02 и 15 3 г / м2 - час. На рис. 63 приведены данные по определению стационарного потенциала титана и сплавов титана с Pt и Pd в насыщенной кислородом и водородом 20 % - ной H2S04 при комнатной температуре [135], а также анодная кривая для титана. [37]
Можно считать, что в большинстве водных растворов стационарный потенциал титана и ряда его сплавов, равный - 0 38 В по водородному электроду, относится к началу пассивации и, следовательно, все потенциалы отрицательнее этого значения характеризуют активное, коррозионно нестойкое состояние. Потенциалы положительнее 0 0В характеризует полностью пассивное и, как правило, коррозионностойкое состояние сплавов. Значение потенциалов между - 0 03 и 0 0 В характеризуют частичную пассивность и неполную стойкость. В табл. 24 даны стационарные потенциалы титана в ряде характерных сред. [38]
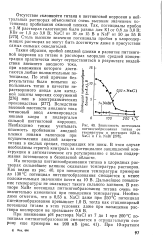 |
Зависимость потенциала питтингообразования титана от температуры в растворах 0 53 н. NaCl и 1 н. NaBr. [39] |
На потенциал питтингообразования титана в хлоридных растворах сильнейшее влияние оказывает температура растворов. Как видно из рис. 40, при повышении температуры примерно до 130 С потенциал питтингообразования смещается к менее положительным значениям почти на 10 В. Дальнейшее повышение температуры не оказывает такого сильного влияния. В растворе NaBr потенциал питтингообразования титана очень незначительно изменяется при повышении температуры. NaCl даже при 250 С потенциал питтингообразования превышает 1 0 В, тогда как стационарный потенциал титана в этих условиях даже при насыщении раствора кислородом не превышает 0 6 В. [40]
Страницы: 1 2 3