Стационарный потенциал - титан
Cтраница 2
Легирование титана хромом не повышает его коррозионной стойкости, а в некоторых случаях даже понижает, так как в серной и соляной кислотах при потенциале, соответствующем стационарному потенциалу титана, хром обладает меньшей склонностью к пассивности, чем титан. [16]
Поверхностное окисление титана в водных растворах протекает легче, чем его растворение. Стационарные потенциалы титана в нейтральных и слабокислых электролитах находятся в положительной области. [17]
Сдвиг потенциалов в отрицательную сторону при повышении концентрации и температуры НС1 указывает на уменьшение коррозионной стойкости. Стационарный потенциал титана в тех же условиях отрицателен и коррозионная стойкость низка. [18]
Титан по значению стационарного потенциала близок к таким металлам, как серебро, нержавеющая сталь и монель-металл. Стационарный потенциал титана в морской воде равен 0 15 в по отношению. [19]
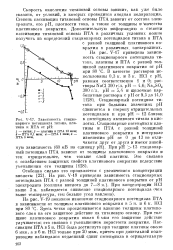 |
Зависимость стационарного потенциала титана, платины и ПТА от рН. [20] |
На рис. V-17 приведена зависимость стационарного потенциала титана, платины и ПТА с разной толщиной платинового покрытия от рН при 80 С. Стационарный потенциал титана при больших значениях рН сдвигается в сторону отрицательных потенциалов и при рН 12 близок к потенциалу активного титана в кислотах. При рН 13 стационарный потенциал ПТА зависит от толщины платинового покрытия и тем отрицательнее, чем тоньше слой платины. [21]
Поверхностное окисление титана в водных растворах протекает легче, чем его растворение. Стационарные потенциалы титана в нейтральных и слабокислых электролитах находятся в положительной области. [22]
 |
Зависимость стационарного потенциала титана, платины и ПТА от рН. [23] |
На рис. V-17 приведена зависимость стационарного потенциала титана, платины и ПТА с разной толщиной платинового покрытия от рН при 80 С. Стационарный потенциал титана при больших значениях рН сдвигается в сторону отрицательных потенциалов и при рН 12 близок к потенциалу активного титана в кислотах. При рН 13 стационарный потенциал ПТА зависит от толщины платинового покрытия и тем отрицательнее, чем тоньше слой платины. [24]
В более агрессивной среде, в 3 н H2SO4, в которой сплав активен, первый максимум отсутствует. В этом растворе стационарный потенциал титана более отрицателен ( - 0 4 в); кривая начинается с потенциала, почти совпадающего со значением первого максимума, наблюдаемого в разбавленной серной кислоте. [25]
В более агрессивной среде, в 3 н H2SO4, в которой сплав активен, первый максимум отсутствует. В этом растворе стационарный потенциал титана более отрицателен ( - 0 4 б); кривая начинается с потенциала, почти совпадающего со значением первого максимума, наблюдаемого в разбавленной серной кислоте. [26]
На рис. 3 представлено влияние непрерывного обновления поверхности на анодную поляризацию титана в растворе IN H2SO4 при наличии воздуха над электролитом. Из приведенных данных видно, что стационарный потенциал титана при непрерывной зачистке его поверхности смещается в отрицательную сторону почти на целый вольт и устанавливается при значении около - 0 7 в. При анодной поляризации для всех исследуемых скоростей обновления ( т 500, 1000, 2000 об / мин) были получены характерные для явления пассивации потенциостатические кривые. Оказалось, что титан даже при зачистке поверхности при всех примененный скоростях обновления переходит в пассивное состояние. Очевидно, пассивное состояние на зачищаемом титане может возникнуть только в том случае, если скорость образования защитного слоя хемосорбированного кислорода будет превышать скорость обновления поверхности. Мы полагаем, что в условиях непрерывной зачистки поверхности причиной перехода титана в пассивное состояние является образование хемосорбированного слоя кислорода, который, однако, при смещении потенциала положительнее Епп может утолщаться. [27]
Основным катодным процессом является водородная деполяризация по реакции ( 2) для кислой среды. Роль кислородной деполяризации мала, так как стационарный потенциал титана в активном состоянии ( от - 0 3 до - 0 7 0) значительно более отрицателен, чем потенциал водородного электрода. В концентрированной серной кислоте, кроме водородной деполяризации, появляется новый катодный процесс - восстановление серной кислоты до молекулярной серы и сероводорода. [28]
При добавлении в метиловый спирт брома, который, как видно из анализа катодных кривых, является катодным деполяризатором, происходит растормаживание контролирующего катодного процесса и, как следствие, сильное снижение коррозионной стойкости титана. Введение в метиловый спирт брома вызывает сдвиг стационарного потенциала титана в положительную сторону ( фиг. [29]
В табл. 3 показано, как изменяется стационарный потенциал титана в зависимости от изменения температуры в 40 % - ном растворе серной кислоты при концентрации 0 3 М ионов четырехвалентного титана. Из данных таблицы видно, что по мере повышения температуры стационарный потенциал титана облагораживается от значения 0 485 в при 0 С до 0 675 в при 100 С, что указывает на повышение защитных свойств пленки. [30]
Страницы: 1 2 3