Наименьший потенциал - ионизация
Cтраница 2
Первые элементы периодов - щелочные металлы - имеют наибольший атомный объем и наибольший радиус атома и наименьший потенциал ионизации по сравнению с остальными элементами соответствующего периода. Водород, будучи первым элементом первого периода, имеет кое-что общее со щелочными металлами. Потенциал ионизации атома Н значительно больше потенциалов ионизации щелочных металлов, а восстановительная способность водорода намного меньше. [16]
Первые элементы периодов - щелочные металлы ( кроме водорода) - имеют наибольший атомный объем и наибольший радиус атома и наименьший потенциал ионизации по сравнению с остальными элементами соответствующего периода. Но Н - ион не имеет аналогов, так как. Потенциал ионизации атома Н значительно больше потенциалов ионизации щелочных металлов, а восстановительная способность водорода намного меньше. [17]
 |
ПМР-спектр пиррол-2 - карбоновой кислоты ( / дм 1 6 Гц, JAX 2 6 Гц, JMX 3 7 Гц. [18] |
При рассмотрении фрагментации азотсодержащих ароматических гетероциклов под действием электронного удара полезно исходить из допущения, что при ионизации молекулы положительный заряд в М локализован на определенном атоме ( или участке) с наименьшим потенциалом ионизации, откуда электрон удаляется легче. Фиксация заряда в определенном месте заметно понижает энергию связи, что способствует ее разрыву. В азотистых гетероциклических соединениях ловушкой положительного заряда в М обычно является гетероатом, поэтому для различных нефункционально замещенных ароматических гетероциклов первая стадия распада М, как правило, связана с выбросом нейтральной частицы HCN. Рассмотрим масс-спектры некоторых соединений. [19]
Величина потенциала ионизации и возбуждения зависит от природы атома. Наименьший потенциал ионизации ( 3 9 э в) имеют пары цезия, а наибольший ( 24 5 э в) наблюдается у газа гелия. У щелочноземельных металлов ( цезия, калия, натрия, бария, кальция) связь между электронами и ядром не велика, поэтому они имеют наименьшие потенциалы ионизации, следовательно, на возбуждение и работу выхода электрона потребуется затратить меньше энергии, чем у железа, марганца, меди и никеля. Элементы, имеющие меньшие потенциалы ионизации и возбуждения, чем свариваемый металл, вводят в состав электродных покрытий, чтобы повысить стабилизацию дугового разряда в газах. [20]
Величина потенциала ионизации и возбуждения зависит от природы атома. Наименьший потенциал ионизации ( 3 9 эВ) имеют пары цезия, а наибольший ( 24 5 эВ) наблюдается у газа гелия. [21]
Величина потенциала ионизации и возбуждения зависит от природы атома. Наименьший потенциал ионизации ( 3 9 э-в) имеют пары цезия, а наибольший ( 24 5 э-б) наблюдается у газа гелия. У щелочноземельных металлов ( цезия, калия, натрия, бария, кальция) связь между электронами и ядром не велика, поэтому они имеют наименьшие потенциалы ионизации, следовательно, на возбуждение и работу выхода электрона потребуется затратить меньше энергии, чем у железа, марганца, меди и никеля. Элементы, имеющие меньшие потенциалы ионизации и возбуждения, чем свариваемый металл, вводят в состав электродных покрытий, чтобы повысить стабилизацию дугового разряда в газах. Количество энергии, которое необходимо для выделения электрона из металла или жидкого тела, называется работой выхода электрона и выражается в электрон-вольтах. [22]
Величина потенциала ионизации и возбуждения за -, втсит от природы атома. Наименьший потенциал ионизации 3 9 э-в) имеют пары цезия, а наибольший ( 24 5 э-в) наблюдается у газа гелия. У щелочноземельных металлов ( цезия, калия, натрия, бария кальция) связь между электронатми и ядром не велика, поэтому они имеют наименьшие потенциалы ионизации. Элементы, имеющие меньшие потенциалы - ионизации и возбуждения, чем свариваемый металл, вводят в состав электродных покрытий, чтобы повысить стабилизацию дугового разряда в газах. Количество энергии, которое необходимо для выделения электрона из металла или жидкого тела, называется работой выхода электрона и выражается в электрон-вольтах. [23]
Цезий обладает наименьшим потенциалом ионизации, поэтому для него можно надеяться получить плазму с высокой концентрацией заряженных частиц при сравнительно низких температурах и достигнуть таким образом высокой степени неидеальности. Экспериментальных данных по уравнению состояния еще не получено, а расчетными данными [26 ] пользоваться нельзя. Дело в том, что при вычислении р ( и) в [26] используется работа [4] без исправления содержащихся там ошибок. Следует отметить, что из-за сравнительно низкой температуры такой плазмы квантовые эффекты в ней будут сказываться в наименьшей мере. [24]
Обычно величина эффективного потенциала ионизации близка по величине к наименьшему потенциалу ионизации одного из компонентов, учас1вующих в смеси дугового газа. Например, при сварке покрытыми элек-гродами, в состав покрытия которых включено легкоионизирующее вещество, содержащее натрий, Тс 810 - 5 1 4131 К, где 5 1-величина потенциала - ионизации натрия. Видно, что при сварке покрытыми электродами температура столба дуги не достигает температуры, необходимой для полной ионизации газов в дуговом промежутке. Поэтому в дуговом промежутке всегда находятся ионы, электроны и неионизированные атомы. [26]
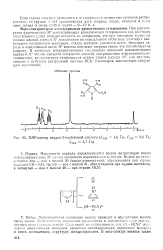 |
ПМР-спектр пиррол-2 - карбоновой кислоты. [27] |
При рассмотрении фрагментации М азотсодержащих ароматических гстероппклов под действием электронного удара полезно исходить из допущения, что при тонизации молекулы положительный заряд в М 1 локализован на определенном атоме ( или участке) с наименьшим потенциалом ионизации, откуда электрон удаляется легче. Фиксация заряда в определенном месте М заметно понижает энергию связи, что способствует ее разрыву. Рассмотрим масс-спектры следующих соединений. [28]
Ионная связь обусловливает образование ионных кристаллов, а также ионных молекул, существующих в парах ионных соединений. Она является следствием электростатического притяжения противоположно заряженных ионов и возникает между атомами, сильно отличающимися потенциалом ионизации и сродством к электрону. Наименьшим потенциалом ионизации обладают атомы щелочных металлов. Отдавая свой внешний электрон, эти атомы превращаются в одновалентные катионы, электронная оболочка которых подобна оболочке атомов инертных газов. Наибольшей энергией сродства к электрону обладают атомы галогенов. Достраивая свою электронную оболочку, эти атомы становятся одновалентными анионами. [29]
Величина потенциала ионизации и возбуждения за -, втсит от природы атома. Наименьший потенциал ионизации 3 9 э-в) имеют пары цезия, а наибольший ( 24 5 э-в) наблюдается у газа гелия. У щелочноземельных металлов ( цезия, калия, натрия, бария кальция) связь между электронатми и ядром не велика, поэтому они имеют наименьшие потенциалы ионизации. Элементы, имеющие меньшие потенциалы - ионизации и возбуждения, чем свариваемый металл, вводят в состав электродных покрытий, чтобы повысить стабилизацию дугового разряда в газах. Количество энергии, которое необходимо для выделения электрона из металла или жидкого тела, называется работой выхода электрона и выражается в электрон-вольтах. [30]
Страницы: 1 2 3
