Наименьший потенциал - ионизация
Cтраница 3
Величина потенциала ионизации и возбуждения зависит от природы атома. Наименьший потенциал ионизации ( 3 9 э в) имеют пары цезия, а наибольший ( 24 5 э в) наблюдается у газа гелия. У щелочноземельных металлов ( цезия, калия, натрия, бария, кальция) связь между электронами и ядром не велика, поэтому они имеют наименьшие потенциалы ионизации, следовательно, на возбуждение и работу выхода электрона потребуется затратить меньше энергии, чем у железа, марганца, меди и никеля. Элементы, имеющие меньшие потенциалы ионизации и возбуждения, чем свариваемый металл, вводят в состав электродных покрытий, чтобы повысить стабилизацию дугового разряда в газах. [31]
Величина потенциала ионизации и возбуждения зависит от природы атома. Наименьший потенциал ионизации ( 3 9 э-в) имеют пары цезия, а наибольший ( 24 5 э-б) наблюдается у газа гелия. У щелочноземельных металлов ( цезия, калия, натрия, бария, кальция) связь между электронами и ядром не велика, поэтому они имеют наименьшие потенциалы ионизации, следовательно, на возбуждение и работу выхода электрона потребуется затратить меньше энергии, чем у железа, марганца, меди и никеля. Элементы, имеющие меньшие потенциалы ионизации и возбуждения, чем свариваемый металл, вводят в состав электродных покрытий, чтобы повысить стабилизацию дугового разряда в газах. Количество энергии, которое необходимо для выделения электрона из металла или жидкого тела, называется работой выхода электрона и выражается в электрон-вольтах. [32]
Для любого атома возможно столько потенциалов ионизации, сколько у него электронов. Потенциал ионизации характеризует способность атома терять свои электроны. Чем ниже потенциал ионизации, тем легче атом теряет свои электроны и тем сильнее у него выражены металлические свойства. Наименьшим потенциалом ионизации обладает цезий. [33]
Более благородные металлы имеют большие потенциалы ионизации, так как из их атомов труднее удаляются валентные электроны. Теплота гидратации иона зависит от его заряда и радиуса. Ионы лития с малым радиусом создают сильное электрическое поле и притягивают ди-польные молекулы воды. При этом выделяется значительная теплота гидратации. Литий - металл с наименьшим потенциалом ионизации и большой теплотой гидратации является наименее благородным металлом. [34]
Простейшим типом химической связи в кристаллах является ионная связь. Ионный кристалл, построенный из атомов двух сортов, состоит из положительно заряженных катионов К и отрицательно заряженных анионов А. Связь ионов в кристалле определяется электростатическим взаимодействием между противоположно заряженными ионами. Расположение ионов в решетке таково, что электростатическое притяжение между катионами и анионами оказывается более сильным, чем электростатическое отталкивание между ионами одинаковых знаков. Ионный тип связи характерен для соединений металлов с металлоидами, поскольку атомы металлов обладают относительно малыми потенциалами ионизации, а атомы металлоидов имеют большое электронное сродство. Наименьшими потенциалами ионизации обладают атомы щелочных металлов: для удаления одного электрона из этих атомов требуется затратить энергию около 5 эв. Наибольшее сродство к электрону имеют атомы галоидов: с присоединением одного электрона к атому галоида выделяется энергия, равная также около 5 эв. Обычно энергия, которую необходимо затратить для образования катиона из нейтрального атома, несколько превосходит энергию, освобождающуюся при образовании аниона, однако этот дефицит в энергии покрывается за счет электростатического взаимодействия катиона и аниона. Структура электронных оболочек ионов, образующих ионный кристалл, характеризуется, как правило, сферически симметричным распределением электронной плотности, что приводит к тому, что ионная связь характеризуется ненасыщаемостью и отсутствием направленности. В связи с этим ионы в решетке ионного кристалла располагаются таким образом, чтобы обеспечить наиболее плотную возможную упаковку. Поскольку ионный кристалл состоит из ионов по меньшей мере двух сортов с различными размерами, то характер этой упаковки зависит от соотношения радиусов ионов. [35]
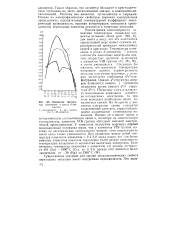 |
Изменение температур плавления в рядах d - эле. [36] |
Рассматривая закономерности изменения температуры плавления элементов вставных декад ( рис. 166), будем иметь в виду, что эта константа в определенной мере может служить характеристикой прочности межатомных связей в кристалле. VIB труппы ( Сг, Mo, W), а затем уменьшается. Следовало бы ожидать, что максимум температуры плавления должен характеризовать металлы подгруппы марганца, у кото - pbfx достигается стабильная d5s2 - KOH-фигурация. Поскольку здесь ргализует-ся максимально возможное количество неспаренных электронов, то при этом возникает наибольшее число ко-валентных связей. На 4s - ypoE e у элементов подгруппы хрома находится единственный электрон, характеризующийся наименьшим потенциалом ионизации. [37]
Страницы: 1 2 3