Коррозионный потенциал
Cтраница 2
 |
Зависимость потен - ся только в случаях возникновения. [16] |
Коррозионные потенциалы меди лежат в области относительно положительных величин и изменяются в зависимости от аэрации и рН раствора. [17]
Измерения коррозионных потенциалов и токов производятся в каждом колодце для соединительных и стопорных муфт и у концевых муфт, а также в специально оборудованных контрольных пунктах, сооружаемых около электрифицированных железных дорог и в других местах с повышенной опасностью коррозионного разрушения оболочек кабелей. [18]
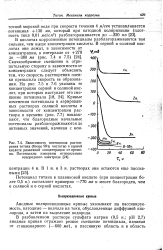 |
Зависимость потенциала растворения титана ( более 99 % чистоты в серной кислоте различной концентрации от времени. Потенциалы измерены относительно водородного электрода. [19] |
В кислотах коррозионные потенциалы разблагораживаются тем сильнее, чем выше концентрация кислоты. Скачкообразное смещение в отрицательную сторону в зависимости от концентрации следует объяснять тем, что скорость растворения пленки превысила скорость ее образования. [20]
Выражения для коррозионного потенциала и плотности тока приведены, как правило, в безразмерном виде, что позволяет использовать их при любых конкретных параметрах систем рассматриваемого вида; при этом для каждой системы указана связь применяемых безразмерных величин с размерными. [21]
Но так как коррозионные потенциалы редко соответствуют нормальным электродным потенциалам, эта классификация зачастую оказывается неверной. [23]
 |
Типы коррозионного контроля. [24] |
Заметим, что коррозионный потенциал в этом случае близок к потенциалу катода разомкнутого контура. Другие примеры - магний, погруженный в воду из природных источников, и железо в растворе хромата. [25]
В аэрированных электролитах коррозионный потенциал металла может лежать значительно положительнее ( катодная поляризационная кривая ghkl, рис. XII. Соответственно к другому значению будет асимптотически приближаться и потенциал стенки трубопровода ( кривая 4, рис. XII. Введение в раствор молекулярного кислорода ( как и любого другого окислителя) затрудняет применение катодной защиты металлов от коррозии и облегчает начальную пассивацию при анодной защите. [26]
По результатам измерения коррозионных потенциалов определяются места установки устройств защиты от блуждающих токов. [27]
Ингибиторы-пассиваторы смещают величину коррозионного потенциала в положителную сторону. Ингибиторы, не являющиеся пассиваторами, оказывают слабое влияние на коррозионный потенциал, и действие их в основном заключается в образовании адсорбционной пленки на поверхности металла. Адсорбция бывает физическая и химическая. Количество адсорбирующегося вещества зависит от его концентрации в среде. Установлено, что выше определенной концентрации вещество адсорбируется хуже. Обычно адсорбционная пленка является мономолекулярной. [28]
Как было сказано выше, коррозионный потенциал и соответствующая ему скорость коррозии зависят от течения не только анодной, но и катодной реакции. [30]
Страницы: 1 2 3 4

