Коррозионный потенциал
Cтраница 3
Изменение режима старения влияет на коррозионный потенциал, потенциал начала пассивации, предельную плотность тока и плотность тока полной пассивации. Две последние величины возрастают при переходе структуры от состояния полного отжига к состоянию полного старения. В кислотных средах мартенситно-стареющие стали могут подвергаться и коррозионному растрескиванию. [31]
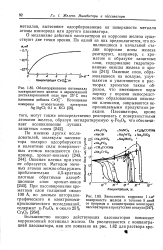 |
Облагораживание потенциала разом, что имеющиеся поры электролитного железа в аэрированной наряду с порами непосредст-дистиллированной воде при 25 С под v 3., . v. [32] |
Большинство анодно действующих пассиваторов повышает коррозионный потенциал железа. [33]
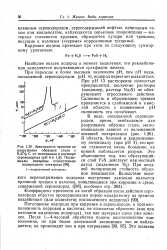 |
Зависимость времени до разрушения образцов стали с 0 47 % С от потенциала в растворе сероводорода ( рН 4 и 1 3. Потенциалы измерены относительно водородного электрода. [34] |
В области, близкой к коррозионному потенциалу ( при рН 4), это время становится очень большим; на кривой наблюдается разрыв. При анодной поляризации стойкость образцов повышается. Вследствие высокого перенапряжения водорода внутренние давления являются причиной трещин и изломов, появляющихся при коррозии в среде, содержащей сероводород ( [98], особенно стр. [35]
Как упоминалось ранее, по коррозионному потенциалу и потенциалу при разомкнутой цепи можно рассчитать коррозионный ток, если известны уравнение поляризации анода или катода и отношение площадей анода и катода. [36]
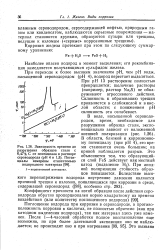 |
Зависимость времени до разрушения образцов стали с 0 47 % С от потенциала в растворе сероводорода ( рН 4 и 1 3. Потенциалы измерены относительно водородного электрода. [37] |
В области, близкой к коррозионному потенциалу ( при рН 4), это время становится очень большим; на кривой наблюдается разрыв. При анодной поляризации стойкость образцов повышается. Вследствие высокого перенапряжения водорода внутренние давления являются причиной трещин и изломов, появляющихся при коррозии в среде, содержащей сероводород ( [98], особенно стр. [38]
Для протекторов пригодны слабополяризующиеся металлы, коррозионный потенциал которых отрицательнее, чем потенциал защищаемого металла. В случае защиты железа этим условиям удовлетворяют цинк, алюминий и магний, а для медных сплавов также и железо. [39]
Эти ионы из-за малости концентрации ( низкие коррозионные потенциалы) оказываются промежуточными частицами процесса (3.14) и потому образование В как по ( 3.14: 1), (3.14.2), так и по (3.14.3) сопровождается одной и той же убылью энергии Гиббса, равной ( гва Цв Согласно (3.16) возникновение - критического зародыша по. [40]
В тех случаях, когда значение коррозионного потенциала близко к равновесному потенциалу одной из сопряженных электрохимических реакций, скорость коррозии металла может быть вычислена путем подстановки выражения для равновесного потенциала в уравнение плотности тока коррозии. [41]
Если скорость коррозии контролируется катодным процессом и коррозионный потенциал близок к потенциалу разомкнутой цепи анодных участков, то необходимая плотность тока только слегка превышает плотность соответствующего коррозионного тока. Но при смешанном контроле требуемый ток может быть значительно больше коррозионного, и он может еще более увеличиваться в случае протекания коррозионных процессов с анодным контролем. [42]
Когда алюминий подвергается анодной поляризации, на естественный коррозионный потенциал накладывается дополнительный потенциал и скорость кор розии увеличивается. Повышенная скорость коррозии способствует увеличению толщины пленки. Электрическое поле уменьшается до первоначального значения. Так как электрически непроводящая пленка имеет небольшую толщину по сравнению с остальной частью пленки, увеличение ее толщины незначительно сказывается на толщине всей пленки и явление поляризации становится понятным. [43]
Наилучший эффект достигается при поляризации до значения коррозионного потенциала активного металла в щели. Достижение этого значения потенциала уменьшает коррозию, но не сводит ее к нулю. [44]
Следовательно, железо, имеющее в морской воде коррозионный потенциал около - 0 4 В, непригодно для использования в качестве протектора для катодно защищаемого алюминия, в отличие от цинка, который имеет более подходящий доррозион-ный потенциал, близкий - 0 8 В. Для нержавеющей стали 18 - 8 критический потенциал в 3 % растворе NaCl равен 0 21 В, для никеля - около 0 23 В. Следовательно, контакт этих металлов с имеющими соответствующую площадь электродами из железа или цинка может обеспечить им в морской воде эффективную катодную защиту, предупреждающую питтинговую коррозию. Элементы создаваемых конструкций ( например, кораблей и шель-фовых нефтедобывающих платформ) иногда специально проектируют таким образом, чтобы можно было успешно использовать гальванические пары такого рода. [45]
Страницы: 1 2 3 4