Коррозионный потенциал
Cтраница 4
На рис. 13 приведена диаграмма, показывающая установление коррозионного потенциала для полностью поляризованного сплава. В отличие от диаграммы Эванса за начальное положение анодных кривых принимается равновесный потенциал каждой структурной еоетавляющей и физически неоднородного участка металла и равновесный окислительно-восстановительный потенциал среды. [46]
По экстраполяции катодной и анодной тафелевских прямых к коррозионному потенциалу ф была получена скорость коррозии iK, заниженная по сравнению с экспериментально найденным значением. [48]
Компромиссный потенциал, который в данном случае называют коррозионным потенциалом, лежит положительнее равновесного цинкового электрода и отрицательнее равновесного потенциала водородного электрода в данных условиях. Таким образом, при компромиссном потенциале баланс зарядов сохраняется благодаря переносу зарядов цинком и водородом, но баланс вещества оказывается нарушенным, что приводит к некоторому, обычно не очень заметному, дрейфу компромиссного потенциала. [49]
Сопоставление полученных значений Kg с литературными данными и значения коррозионных потенциалов свидетельствуют что все исследованные металлы находятся в пассивном состоянии. Коэффициенты KB для латуни и припоя определены впервые. При исследовании кинетики коррозии металлов в антифризе при 70 и 90 С показано что скорость коррозии вначале уменьшается, достигая постоянных значений за 30 - 40 ч при 70 С и 2 - 4 ч при 90 С. [50]
Сопоставление полученных значений Kg с литературными данными и значения коррозионных потенциалов свидетельствуют, что все исследованные металлы находятся в пассивном состоянии. Коэффициенты KB для латуни и припоя определены впервые. При исследовании кинетики коррозии металлов в антифризе при 70 и 90 С показано, что скорость коррозии вначале уменьшается, достигая постоянных значений за 30 - 40 ч при 70 С и 2 - 4 ч при 90 С. [51]
Итак, в естественных условиях потенциал металла - это его коррозионный потенциал, который определяется характером анодной и катодной реакций, образующих суммарную коррозионную реакцию. [52]
Склонность к пассивности выражается уже благородными ис - ходными значениями коррозионного потенциала. Вещества, образующие комплексные соединения, устраняют пассивность. Например, добавляемые к азотной кислоте ионы F - вызывают этот эффект уже при незначительных концентрациях ( табл. 7.4, стр. В серной и соляной кислотах при более высоких концентрациях пассивирования также не происходит, так как образуются комплексные сульфо - и хлоротитановые соединения ( ср. [53]
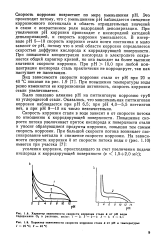
Это происходит потому, что с уменьшением рН наблюдается смещение коррозионного потенциала в область отрицательных значений в связи с возрастанием роли водородной деполяризации. При увеличении рН коррозия происходит с кислородной катодной деполяризацией, и скорость коррозии уменьшается. В интервале рН 5 - 10 скорость коррозии стали почти постоянна и мало зависит от рН, потому что в этой области коррозия определяется скоростью диффузии кислорода к корродирующей поверхности. При повышении концентрации кислорода в электролите сохраняется общий характер кривой, но она выходит на более высокие значения скорости коррозии. При рН 10 0 при любой концентрации кислорода сталь практически не корродирует, так как наступает ее пассивация. [55]
Склонность к пассивности выражается уже благородными ис - ходными значениями коррозионного потенциала. Вещества, образующие комплексные соединения, устраняют пассивность. Например, добавляемые к азотной кислоте ионы F - вызывают этот эффект уже при незначительных концентрациях ( табл. 7.4, стр. В серной и соляной кислотах при более высоких концентрациях пассивирования также не происходит, так как образуются комплексные сульфо - и хлоротитановые соединения ( ср. [56]
Страницы: 1 2 3 4