Окислительно-восстановительный потенциал - система
Cтраница 2
Окислительно-восстановительный потенциал системы лю-циферин-оксилюциферин пока не измерен. Оксилюциферин не может быть восстановлен гидросульфитом или водородом с платиной. [16]
 |
Типичные кривые потенциометри. [17] |
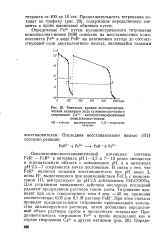
Окислительно-восстановительный потенциал системы FeR - - FeR2 - в интервале рН 1 - 2 5 и 7 - 10 резко смещается в отрицательную область с повышением рН, а в интервале рН 2 5 - 7 сохраняется почти постоянным. Для устранения мешающего действия кислорода последний удаляют продуванием раствора током азота. При этом сначала проводят предварительное титрование произвольного количества анализируемого раствора, затем добавляют определенный объем раствора пробы и продолжают титрование. [18]
Окислительно-восстановительный потенциал системы Ag / Ag равен 0, 80 в, поэтому кислоты, которые не являются окислителями, не растворяют серебра. [19]
Окислительно-восстановительный потенциал системы Ag 2 / Ag равен 1 98 в, поэтому соли двухвалентного серебра чрезвычайно неустойчивы и являются сильными окислителями, например: Ag2 окисляет Мп11 в Mnv на холоду; РЬП в PbIV - при нагревании. [20]
Окислительно-восстановительный потенциал системы Hg / Hg равен 0 80 в. Следовательно, ртуть не растворяется в соляной и разбавленной серной кислотах. Ртуть легко растворяется при нагревании в азотной и концентрированной серной кислотах, а также в царской водке. [21]
Окислительно-восстановительный потенциал системы РЬ / 2 РЬ в кислой среде равен - 0 13 в, поэтому свинец должен растворяться в разбавленных соляной и серной кислотах. Однако образующиеся при этом на поверхности металла хлорид и сульфат свинца нерастворимы в воде и поэтому предохраняют металл от дальнейшей коррозии. В концентрированной H2SO4 свинец растворяется, так как образуется растворимая в воде кислая соль Pb ( HSO4) 2, не защищающая свинец от действия кислоты. Свинец растворяется в разбавленной HNO3 и не растворяется в концентрированной HNO3, так как образующиеся при этом на поверхности металла окислы свинца предохраняют металл от действия кислоты. [22]
 |
Формы нахождения сурьмы ( III в растворе в зависимости от рН. [23] |
Окислительно-восстановительный потенциал системы SbO - / Sb в кислой среде равен 0 21 в; в щелочной среде потенциал системы SbOjT / Sb равен - 0 67 в. Поэтому сурьма нерастворима в разбавленных серной и соляной кислотах и растворяется при нагревании в едких щелочах; при этом образуются метастибиты. [24]
Окислительно-восстановительные потенциалы систем Mo ( VI) / Mo ( V) и Мо ( Т) / Мо ( ШХ - Журн. [25]
Окислительно-восстановительный потенциал системы Ag / Ag равен 0 80 в, поэтому кислоты, которые не являются окислителями, не растворяют серебра. [26]
Окислительно-восстановительный потенциал системы РЬ / 2 РЬ в кислой среде равен-0 13 в, поэтому свинец должен растворяться в разбавленных соляной и серной кислотах. Однако образующиеся при этом на поверхности металла хлорид и сульфат свинца нерастворимы в воде и поэтому предохраняют металл от дальнейшей коррозии. [27]
 |
Формы нахождения сурьмы ( III в растворе в зависимости от рН. [28] |
Окислительно-восстановительный потенциал системы SbO / Sl: в кислой среде равен 0 21 в; в щелочной среде потенциал системы SbO7 / Sb равен - 0 67 в. Поэтому сурьма нерастворима в раз бавленных серной и соляной кислотах и растворяется при нагревании в едких щелочах; при этом образуются метастибиты. [29]
Окислительно-восстановительный потенциал системы FeOl - / Fe3 в сильнокислой среде ( рН0) превышает 1 9 в. В щелочной среде потенциал находится между 0 6 - 0 7 в. Известны только ее соли - ферраты. [30]
Страницы: 1 2 3 4