Межмолекулярный потенциал
Cтраница 2
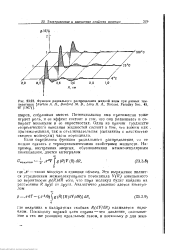 |
Функция радиального распределения жидкой воды при разных температурах [ Norten А. И., Danford M, .., Levy H. Л., Discuss. Faraday Soc., 43, 97 ( 1907 ]. [16] |
Это выражение является усреднением межмолекулярного потенциала V ( R) взвешенного 1: 0 вероятности g ( R) dR того, что пара молекул будет найдена на расстоянии R Друг от Друга. [17]
Это выражение является усреднением межмолекулярного потенциала V ( R) взвешенного iio вероятности g ( R) dR того, что пара молекул будег найдена на расстоянии R друг от друга. [18]
Это выражение являет-я усреднением межмолекулярного потенциала V ( R) взвешенного о вероятности g ( R) dR того, что пара молекул будег найдена на асстоянии R друг от друга. [19]
Попытка вычислить силовые постоянные межмолекулярного потенциала Леннарда-Джонса на основании этих экспериментальных значений В оказалась неудачной. Причина этой неудачи в настоящее время не ясна. [20]
Рассмотрен вопрос об использовании эффективного межмолекулярного потенциала взаимодействия полярных веществ, полученного усреднением, реального, зависящего от ориентации молекул, потенциала по углам, при. [21]
Впоследствии оказалось, что применение межмолекулярных потенциалов к органическим кристаллам мало что дает, поскольку для описания взаимодействия таких молекул, как, скажем, метан или бензол, требовались бы различные потенциальные кривые. Расчет взаимодействия молекул сводится в этом случае к суммированию атомных взаимодействий по всем парам атомов, принадлежащих рассматриваемым молекулам. Такой подход оказался исключительно плодотворным для предсказания строения и свойств органических кристаллов. [22]
Связь между вириальными коэффициентами и межмолекулярным потенциалом в математической форме довольно сложна, н принцип метода и выражение для В ( Т) совершенно четкие. [23]
 |
Классификация межмолокулярных взаимодействий. [24] |
На рис. 1.2 изображен типичный вид межмолекулярного потенциала и приведена классификация взаимодействий в различных областях межмолекулярных расстояний. [25]
Применение высокоэнергетических молекулярных пучков для нахождения межмолекулярных потенциалов обязано пионерским исследованиям Амдура с сотрудниками 1114J в США и грунны Леоиаса 1110J в СССР. Из недавних работ упомянем работы 1115, 11UJ, Обработка экспериментальных данных, как правило, может быть проведена в классическом приближении и дает отталкивательную часть потенциальной кривой, которая аппроксимируется либо потенциалом Бор на - Майора, либо сте-неппой зависимостью Сп / гп. [26]
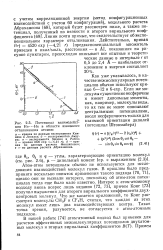 |
Потенциал взаимодейст взаимной ориентации диполей вия Не - - - Не в области взаимного ( потенциал Штокмайера отталкивания атомов. [27] |
Как уже указывалось, в качестве межмолекулярных потенциалов обычно используют кривые 6 - 12 и 6-ехр. [28]
В этой главе в приближении разделения межмолекулярного потенциала на потенциал притяжения и отталкивания рассматриваются отдельные составляющие потенциала взаимодействия двух молекул воды. Термодинамические свойства пара и вязкость пара сравниваются с аналогичными свойствами F S, так же как в гл. [29]
Полином (20.3) представляет собой приближение для широко используемого межмолекулярного потенциала Ленарда - Джонса. [30]
Страницы: 1 2 3 4