Замена - заместитель
Cтраница 2
D практически не оказывает влияния на реакцию, тогда как другие тесты, такие, как замена заместителя или изменение полярности растворителя, могут оказывать более сложное действие. [16]
Совместное рассмотрение этих двух эффектов дает вполне удовлетворительную основу для качественной характеристики поведения большинства карбонильных частот при замене заместителей при атоме углерода карбонильной группы. Исключения составляют те случаи, когда проявляется связь колебаний или эффекты изменения валентных углов, а также особые случаи эффектов поля, которые будут рассмотрены ниже. Когда частоты выше, чем карбонильная частота ацетона в той же среде, соответствующие соединения могут рассматриваться как соединения, индукционный эффект которых превосходит любые резонансные эффекты. Обратное утверждение верно для более низких частот. Такое разделение справедливо не только в простых случаях ( высокая частота ацетилхлорида или низкая частота ацетамида), но также и в более сложных случаях. Аналогично высокие частоты колебаний СО виниловых эфиров по сравнению с алкильными сложными эфирами обусловлены, вероятно, конкуренцией между карбонильной группой и олефиновой двойной связью за неподеленную пару электронов атома кислорода. [17]
Таким образом, изменения в структуре радикала как за счет появления новых связей, так и при замене заместителей приводят к изменениям молекулярных орбит неспаренного электрона. [18]
Эфиры салициловой кислоты - эффективные УФ-абсорберы, обычно имеющие одну полосу поглощения в области 312 нм, положение которой не меняется при замене заместителей в фенильном ядре, связанном с 2-оксибензолом кислородным мостиком. [19]
Химические эффекты обычно подразделяют на индукционные, резонансные ( или мезомерные) и эффекты поля, и в общем изменение карбонильной частоты при замене заместителя X может быть удовлетворительно объяснено влиянием этих эффектов. Если заместитель X заменен другим заместителем, имеющим большую способность притягивать электроны, то формальный положительный заряд на атоме кислорода повышается. Это снижает различие в способности притягивать электроны между атомами углерода и кислорода, и полярность связи уменьшается. Так как ионные радиусы больше ковалентных, связь укорачивается и vCO увеличивается. Обнаружено также, что соединения с более высокими значениями vCO менее чувствительны к влиянию природы растворителя или фазовым изменениям ( по крайней мере в отношении значения vCO), тогда как соединения с малыми значениями карбонильных частот проявляют значительную чувствительность к этим эффектам. [20]
Метиловый красный характеризуется формулой, подобной формуле метилового оранжевого, за исключением того, что сульфогруп-па в кольце заменена на карбоксильную группу. Замена заместителей у азота аминогруппы и в кольце приводит к получению ряда индикаторов со слегка отличающимися свойствами. [21]
Для получения хромоксановых красителей из группы о-крезотиновой кислоты более высокого цвета, чем голубой, необходимо ввести в молекулу второй ЭД-заместитель. Удобнее всего это осуществляется заменой подвижного заместителя в пара-положении к центральному атому углерода. [22]
Для получения хромоксановых красителей ( из группы о-крезотиновой кислоты) более высокого цвета, чем голубой, необходимо ввести в молекулу второй ЭД-заместитель. Удобнее всего это осуществляется заменой подвижного заместителя в пара-положении к центральному атому углерода ( как при синтезе Кислотного ярко-синего из Кислотного зеленого для кожи, см. стр. [23]
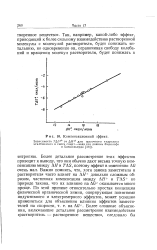 |
Компенсационный гффект. [24] |
Более детальное рассмотрение этих эффектов приводит к выводу, что они обычно дают весьма точную компенсацию между ДЯ и ГД5, поэтому эффект в изменении Дй очень мал. Важно помнить, что, хотя замена заместителя и растворителя часто влияет на ДЯ довольно сложным образом, частичная компенсация между ДЯ и ГД5 по природе такова, что их влияние на ДО оказывается много проще. [25]
Таким образом, можно предположить, что реакция протекает либо по механизму Е2, либо по механизму ElcB. Однако значительное изменение изотопного эффекта при замене заместителя в сульфонатной группе маловероятно, так как влияние заместителя должно сильно гаситься при передаче через 7 атомов. [26]
Необходимо рассмотреть применимость уравнения Гаммета для корреляции со структурой соединений скоростей таких реакций, при которых в зависимости от типа заместителя или природы растворителя происходит частичное или полное изменение механизма. Классическим примером реакций, протекающих с изменением механизма при замене заместителя в пределах одной реакционной серии, являются реакции нуклеофильного замещения атома галогена в арилг алогенидах. [27]
Другой причиной снижения скорости реакции является изменение реакционной способности промежуточных продуктов окисления. Последовательное окисление метильных групп приводит, по - существу, к замене донорных заместителей ( - СН3) на акцепторные ( - GOOH) и, в зависимости от количества последних, а также от их относительного положения реакционная способность промежуточных продуктов будет существенно различаться как между собой, так и по сравнению с таковой у исходного углеводорода. В связи с этим по мере изменения состава реакционной массы в ходе окисления необходимо изменять условия проведения реакции. [28]
У неплоских структур, таких, как пирамидальные фосфаты и сульф-оксиды, возможность проявления этого эффекта соответственно сильно уменьшена, и этим объясняется относительная независимость частот колебаний групп Р О и S О от эффектов сопряжения. Поэтому индукционный эффект является основным фактором, обусловливающим изменения этих частот при замене заместителей. Бел-лом и др. [47] показано, что у галогенидов фосфорила частота колебаний Р О является линейной функцией суммы электроотрицательностей атомов галогенов. Им удалось также для групп атомов других заместителей получить значения электроотрицательностей, которые, по-видимому, могут успешно применяться для этого ряда соединений, хотя для заместителей ОН и NH2 имеются некоторые неточности, обусловленные, по-видимому, наложением эффектов водородной связи. [29]
Однако у системы с преобладающей ковалентной формой такое замещение может приводить к понижению более высокой частоты, так как частоты NC и CS должны разделяться больше, и их взаимодействие при замещении будет уменьшаться. Таким образом, направление смещения частоты vas систем XYZ не может дать полезной информации об изменениях полярности при замене заместителей до тех пор, пока окончательно не выяснится природа участвующих связей. [30]
Страницы: 1 2 3