Первый ионизационный потенциал
Cтраница 1
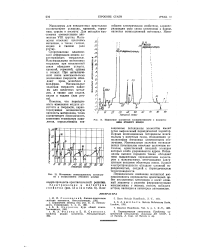 |
Изменение ионизационного потенциала с возрастанием атомного номера.| Изменение магнитной восприимчивости с возрастанием атомного номера. [1] |
Первые ионизационные потенциалы максимальны у инертных газов, обладающих заполненными внешними электронными оболочками. Минимальные значения ионизационных потенциалов отвечают щелочным металлам, единственный внешний электрон которых слабо удерживается ядром. Потенциалы высших порядков также обладают ярко выраженным периодическим характером с максимумами, отвечающими завершенным внешним оболочкам ионов. Кривая электропроводности обладает сложной периодичностью, сходной с периодичностью теплопроводности. [2]
Первый ионизационный потенциал радона равен 10 6 эв и второй - 19 9 эв. [3]
 |
Физические свойства металлического полония. [4] |
Первый ионизационный потенциал полония равен 8 43 в, энергия диссоциации молекулы Ро2 - 1 895 эв. [5]
Первые ионизационные потенциалы радикалов являются мерой легкости их окисления в карбониевые ионы ( или восстановления ионов карбония в радикалы) и при соответствующем учете эффектов сольватации могут быть связаны с этими реакциями в растворах. Поэтому полярографические потенциалы полуволны для восстановления карбониевых ионов должны каким-то образом зависеть от ионизационных потенциалов, но пока имеется мало измерений для надежной проверки этого предсказания ( разд. [6]
 |
Конфигурации из атомов бора в структурах борпдов. [7] |
Первые ионизационные потенциалы легких неметаллов составляют: В 8 28; С 11 24; N 14 51; О 13 57; Si 8 14, Р 10 43; S 10 42 эв. В соответствии с этим следует ожидать, что для заполнения с. Поэтому бориды и силициды переходных металлов должны обладать наименьшей хемосорбционной и каталитической активностью, причем это понижение должно увеличиваться с ростом акцепторной способности переходного металла. При переходе к карбидам, фосфидам и сульфидам следует ожидать не понижения, а напротив, повышения каталитической активности по сравнению с переходными металлами. Это обусловлено частичным переходом d - электронов металла в общий электронный коллектив с уменьшением степени достроенное с. Эти закономерности должны существенно усложняться при образовании атомами неметаллов обособленных структурных элементов кристаллической решетки, как это, в частности, происходит для боридов и силицидов. [8]
У большинства атомов первый ионизационный потенциал лежит в пределах от 5 до 10 в, что должно соответствовать образованию в процессе ионизации нового кулонов-ского поля па расстоянии примерно от 1 А до бесконечности. Электростатическая энергия кулоновского поля приблизительно равна 7 / г эв, если г измеряется в ангстремах. [9]
Еще ниже - первые ионизационные потенциалы элементов ряда натрий-франций вследствие того, что заполненная 2 / 6-оболочка их ионов наиболее сильно экранирует заряд ядра. [10]
По теореме Купманса, первые ионизационные потенциалы могут быть отождествлены с энергией высшей занятой ороитали. Поэтому рассмотренные примеры следует считать. [11]
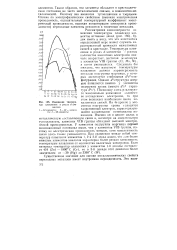 |
Изменение температур плавления в рядах d - эле. [12] |
У элементов подгруппы марганца первый ионизационный потенциал выше, чем у элементов VIB труппы, поэтому их электрическая проводимость меньше, хотя ковалентность связи здесь также уменьшается. При сравнении между собой температур плавления элементов 1, 2 и 3 - й декад видно, что для более тяжелых элементов-аналогов характерна более резкая зависимость температуры плавления от / количества валентных электронов. [13]
В табл. 5 приведены рассчитанные первые ионизационные потенциалы ( ИП) кластерных карбонилов, которые по теореме Купманса приравниваются к электронной энергии верхней занятой молекулярной орбитали. [14]
На основании УФ-спектров заключают, что первый ионизационный потенциал диборана равен 11 - 12 эв. [15]
Страницы: 1 2 3 4