Наблюдаемый потенциал
Cтраница 2
Вычисления по формулам ( 14.11 - 14.26) приводят к данным, совпадающим с экспериментально наблюдаемыми потенциалами, только в случае термодинамически обратимых редоксипар и при отсутствии смешанных потенциалов. [16]
Серебро, будучи более благородным металлом, чем ртуть, имеет в большинстве электролитов потенциал восстановления более положительный, чем потенциал анодного растворения ртути, поэтому наблюдаемый потенциал восстановления серебра фактически является потенциалом анодного растворения ртути. [17]
Образование в катодных процессах Ti ( II) дли металлического, Ti мало вероятно из-за высоких отрицательных значений потенциалов систем Ti ( III) - Ti ( II); Ti ( III) - Ti; Ti ( IV) - Ti ( II); Ti ( II) - Ti [25] не соответствующим реально наблюдаемым потенциалам. [18]
Неудовлетворительное функционирование платинового индикаторного электрода при титровании четырехвалентного титана связано с тем, что при потенциале раствора ниже потенциала системы Н2 / 2Н ( - 0 24 в в Ш НС1 относительно насыщенного каломельного электрода) на его поверхности ускоряется протекание реакции: 2Сг2 2Н 2Сг3 Н2, вследствие чего фактическое отношение концентраций [ Сг3 ] / [ Сг2 j на поверхности электрода становится значительно меньшим, чем в массе раствора, а наблюдаемый потенциал соответственно этому становится более положительным, чем истинный потенциал. Иными словами, платиновый электрод функционирует частично как водородный электрод, а наблюдаемый потенциал находится между потенциалами систем Н2 / 2Нн и Сг / Сгш. [19]
Многие реакции электролиза не являются обратимыми. Наблюдаемый потенциал разложения превышает величину, вычисляемую из термодинамических данных. Этот избыточный потенциал, называемой потенциалом перенапряжения, зависит от площади электродов и состояния их поверхности, наличия примесей в растворе и плотности тока, протекающего через раствор. [20]
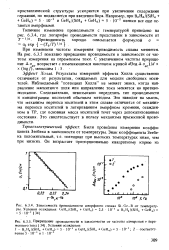
Результаты измерений эффекта Холла существенно отличаются от результатов, ожидаемых для модели свободных носителей. Наблюдаемый потенциал Холла не меняет знака, когда направление магнитного поля или направление тока меняется на противоположное. Следовательно, невозможно определить тип проводимости и концентрацию носителей обычным методом. Это наводит на мысль, что механизм переноса носителей в этом сплаве отличается от механизма переноса носителей - в легированном аморфном кремнии, осажденном в ТР, где основная масса носителей течет через делокализованные состояния. Это свидетельствует в пользу механизма прыжковой проводимости. [22]
Плотность тока i на кривых 4 и 5 отвечает одному и тому же электрохимическому процессу. Поэтому при наблюдаемом потенциале е, с учетом TIOM электродный процесс 1, а при к 2 - процесс 2 находятся в равновесии. [24]
В некоторых экспериментах растворы приводятся в соприкосновение и бок о бок перемещаются на некоторое расстояние. Иногда предполагается, что наблюдаемые потенциалы должны приблизительно совпадать с потенциалами в случае границы со свободной диффузией. [25]
Таким образом, металлическая медь является более слабым восстановителем, чем цинк, или кадмий, или ион водорода. Как и прежде, наблюдаемый потенциал является количественной мерой восстановительной способности. [26]
В некоторых экспериментах растворы приводятся в соприкосновение и бок о бок перемещаются на некоторое расстояние. Иногда предполагается, что наблюдаемые потенциалы должны приблизительно совпадать с потенциалами в случае границы со свободной диффузией. [27]
Потенциалы разложения, определяемые в реальных условиях электролиза, больше разности стандартных потенциалов электродов. Величина, на которую наблюдаемый потенциал разложения превышает равновесный потенциал ( в условиях обратимости процесса), называется перенапряжением при электролизе. Перенапряжение, следовательно, связано с термодинамической необратимостью процесса в реальных условиях электролиза. [28]
Простейшая схема решения этой задачи состоит в использовании эффективных зарядов ядер. Последние выбираются в соответствии с наблюдаемыми потенциалами ионизации 17 42 эв для фтора и 12 13 эв для ксенона. Получающиеся в результате эффективные заряды имеют величины, несколько превышающие единицу как в случае фтора, так и в случае ксенона. Это приводит к неестественному отсутствию электронейтральности молекулы в целом. [29]
Снимают полярографическую кривую; потенциал восстановления никеля 0 95 в, меди - 0 35 в. При употреблении сульфита для удаления кислорода наблюдаемые потенциалы становятся более положительными. Высоту полярографической волны испытуемого раствора сравнивают с высотой волны стандартного раствора. [30]
Страницы: 1 2 3 4