Наблюдаемый потенциал
Cтраница 3
Неудовлетворительное функционирование платинового индикаторного электрода при титровании четырехвалентного титана связано с тем, что при потенциале раствора ниже потенциала системы Н2 / 2Н ( - 0 24 в в Ш НС1 относительно насыщенного каломельного электрода) на его поверхности ускоряется протекание реакции: 2Сг2 2Н 2Сг3 Н2, вследствие чего фактическое отношение концентраций [ Сг3 ] / [ Сг2 j на поверхности электрода становится значительно меньшим, чем в массе раствора, а наблюдаемый потенциал соответственно этому становится более положительным, чем истинный потенциал. Иными словами, платиновый электрод функционирует частично как водородный электрод, а наблюдаемый потенциал находится между потенциалами систем Н2 / 2Нн и Сг / Сгш. [31]
Чтобы найти точные значения для связей углерод-галоген с учетом потенциала появления иона СРз ( определенного при работе с трифторметилгалогенидами), Дайблер, Риз и Молер27 предложили значение 9 3 эв. С другой стороны, Прайс5 отдает предпочтение величине 9 5 эв, которая согласуется с наблюдаемыми потенциалами ионизации других подобных же радикалов. Ионизационные потенциалы двух таких радикалов недавно измерены Лоссингом28 при помощи метода прямого электронного удара. [32]
Во многих преобразователях энергии и в некоторых аккумуляторах в качестве окислителя используется кислород или воздух. Поэтому в случае простой системы кислородно-водородного топливного элемента с платиновыми электродами в отсутствие тока или при низких плотностях тока отличие наблюдаемого потенциала от теоретического обусловлено в основном поляризационными потерями на кислородном электроде, а водородный электрод работает практически в равновесных условиях. Потери по мощности в случае предельно низких плотностей тока составляют 20 - 30 % теоретической величины, а в практических условиях работы топливного элемента - еще выше. Кислородные электроды из других металлов ведут себя в кислых и щелочных растворах подобным же образом. Любое усовершенствование кислородных электродов, например в результате разработки новых, лучших электрокатализаторов для реакции ионизации кислорода, означает улучшение характеристик систем топливных элементов или аккумуляторов энергии. В связи с этим в последнее время особое внимание уделяется изучению реакций ионизации кислорода на разных электродах, а также исследованию и разработке новых, лучших катализаторов. [33]
Ошибки в экспериментальных данных в настоящее время не поддаются определению. Они возникают из-за неточностей в вычислении энергии сольватации ароматического иона и абсолютного потенциала электрода, а также из-за разницы между наблюдаемым потенциалом полуволны и обратимым потенциалом присоединения электрона к молекулам. Это может служить какой-то оценкой величины ошибки в ходе эксперимента. [34]
 |
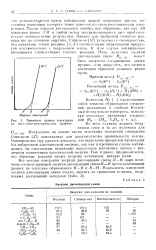
Электрохимические реакции, характеризующие особенности равновесия системы Ti - Н20. [35] |
Анализ данных, приведенных в табл. 2.9 и на рис. 2.9 [31], свидетельствует о том, что процессы образования оксидов и пассивации титана непросты. В частности, нельзя строить модель пассивации титана на предположении об образовании пассивирующего слоя оксидов в результате взаимодействия атомов титана и молекул воды, поскольку нормальные потенциалы для: всех известных оксидов титана значительно отрицательнее наблюдаемого потенциала пассивации титана. [36]
Анализ приведенных данных показывает, что процессы окис-лообразования и пассивации титана не могут быть простыми. В частности, приходится отбросить предположение о возможности образования пассивирующего окисла в результате обычных реакций с участием атомов титана и молекул воды, так как отвечающие им нормальные потенциалы для всех известных окислов титана значительно отрицательнее наблюдаемого потенциала пассивации титана. Причина такого явления лежит в том, что поверхность титана всегда покрыта гидридным слоем, и в реакциях с водой участвует не сам титан, а его гидрид. В работе [26] показано соответствие электрохимического поведения титана и гидрида TiH2 в растворе H2SO4, в частности практически совпадают потенциалы их пассивации. [37]
Как известно, разряд ионов Н лишь на платинированной платине при малых плотностях тока происходит при потенциалах, близких к равновесному. На других же материалах разряд происходит при потенциалах, значительно более отрицательных. Разность между равновесным и наблюдаемым потенциалом разряда иона называется перенапряжением. Величина перенапряжения зависит от многих причин и в первую очередь от качества материала электрода, состояния его поверхности, плотности тока, температуры и пр. [38]
Однако на опыте не удается получить электрод, показания которого были бы воспроизводимы и соответствовали теоретически подсчитываемым величинам. Так, например, при насыщении платины кислородом получаются потенциалы, которые сильно отличаются от теоретических величин и плохо воспроизводятся. В табл. 40 приведены экспериментально наблюдаемые потенциалы такого кислородного электрода. [39]
С практической точки зрения использование стандартных электродных потенциалов ограничено. Хотя электродный потенциал легко измерить, часто его нельзя перевести в стандартный электродный потенциал из-за отсутствия данных об активностях. Формальный потенциал представляет собой экспериментально наблюдаемый потенциал в растворе, содержащем равные молярные концентрации форм Ох и Red. Такое выражение концентрации не дает никакой информации о концентрации молекулярных и ионных частиц, действительно присутствующих в растворе. [40]
 |
Энергия диссоциации связи. [41] |
Таким образом уменьшается ошибка при обработке, так как ЛВ примерно равно А В и любой метод экстраполирования дает приблизительно эквивалентные результаты. Однако для требуемой точности разница все же слишком ощутима. Стивенсон [47] установил с очевидностью, что начальные точки разрыва ( Л, А) соответствуют образованию продуктов исключительно с выделением тепла. В этом случае наблюдаемые потенциалы соответствуют теплоте реакции. [42]
В действительности, наблюдаемые потенциалы ионизации бутена-2 и изобутилена очень близки. Именно это расхождение и было одной из причин, которые заставили Стрейтвизера и Найра отвергнуть индуктивную модель. Аналогичная трудность возникает в случае ксилолов, где метод Хюккеля предсказывает значительно больший потенциал ионизации для жега-изомера, чем для двух остальных. В действительности же наблюдаемые потенциалы ионизации всех трех изомеров очень близки. Эти соображения показывают, что причиной неуспеха индуктивной модели Хюккеля может быть просто то обстоятельство, что она переоценивает поляризуемости связей и что лучшим приближением может быть полное пренебрежение индуктивной поляризацией я-электронов под влиянием алкильных заместителей. [43]
Как следует из табл. 13.1 и 13.2, достижение предельно высоких анодных потенциалов, помимо использования тетрафтор-боратов и гексафторфосфатов, возможно при понижении температуры [59] или при использовании таких растворителей, как трифторуксусная [60, 67, 68] и фторсульфоновая [57, 69-72] кислоты. Наблюдавшиеся потенциалы в случае необратимого окисления постоянны, и их можно предсказать. Во многих случаях эти потенциалы хорошо коррелируют с потенциалами ионизации [56, 58, 74] и с константами о [63, 64]; в последнее время потенциалы ионизации обычно измеряют методом фотоэлектронной спектроскопии. Общая тенденция изменения потенциалов окисления может быть выведена исходя нз структур углеводородов на основе механизма, включающего перенос электрона с последующим быстрым разрывом связей углерод-водород или углерод-углерод Для таких случаев на наблюдаемый потенциал влияет скорость последующей реакции. С этим связаны относительно низкие потенциалы окисления напряженных углеводородов, катнои-радикалы которых, как можно ожидать, способны подвергаться фрагментации ( см табл 13 4) Таким же образом можно объяснить низкий потенциал окисления цикло-гексадиена-1 4 ( см. табл. 13.3); в этом случае быстрое отщепление протона катион-радикалом приводит к цнклогексаднениль-ному радикалу. [44]
Эти опыты были продолжены г-жой Вертенштейн [5] с целью изучить, как влияют концентрации полония и азотной кислоты в растворе на значения потенциала выделения. Применявшийся этим автором метод в принципе одинаков с методом Хевеши и Панета. Эти новые исследования показали, что потенциал выделения не зависит от концентрации полония и кислоты. Отсюда автор заключил, что закон Нернста в этом случае более не применим, и поэтому он интерпретировал этот результат, исходя из предположения, что значения наблюдаемых потенциалов выделения определяются электрохимическими свойствами твердых растворов в золоте продуктов, разряжающихся на электродах. [45]
Страницы: 1 2 3 4